El dominio de Novo Nordisk en el ámbito de la diabetes y la obesidad se ha visto comprometido.
La tirzepatida, un agonista dual de GLP-1 y GIP desarrollado por Eli Lilly, se ha postulado como el rey en términos brutos de pérdida de peso. La serie de ensayos clínicos SURMOUNT, destinados a probar la eficacia de la tirzepatida para controlar el sobrepeso y la obesidad, han demostrado que los pacientes con las dosis más altas de tirzepatida perdían más de un 20% de peso de media.
Eso comparado con el 15 % de pérdida de peso que provoca la semaglutida.
Si yo fuera Novo Nordisk, estaría nervioso.
Pero la compañía danesa tiene un as bajo la manga.
(Realmente tiene varios, pero hoy nos centraremos en uno de ellos).
Hoy vengo a hablar de CagriSema, la nueva gran apuesta de Novo.
¿Será este fármaco lo suficientemente bueno para destronar a la tirzepatida?
Al lío.
CagriSema, un fármaco dual.
Bajo el nombre de CagriSema se esconden dos compuestos pensados para actuar de manera conjunta: semaglutida y cagrilintida.
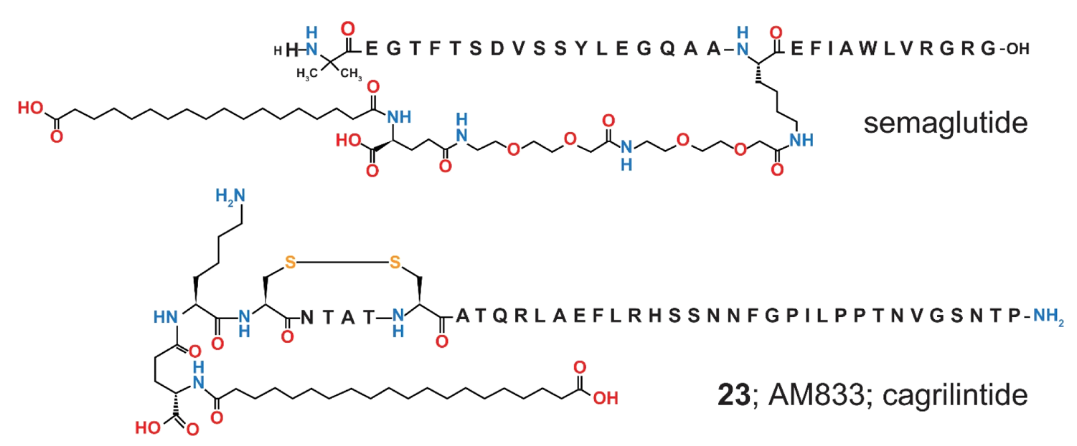
¿Qué es la cagrilintida? Para responder a esta pregunta tendremos que entender primero a quién trata de emular este fármaco: la amilina.
Amilina
La amilina es un péptido de 37 aminoácidos producido por las células del páncreas en situaciones normales. Su estructura es la típica de las hormonas peptídicas, una cadena sencilla de aminoácidos que forman una hélice para unirse a su receptor.
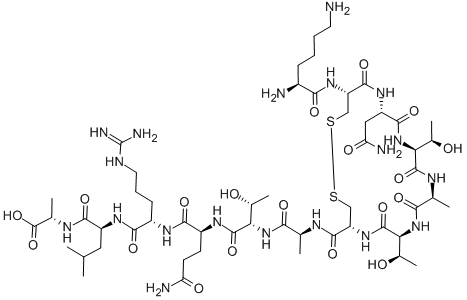 Estructura de la amilina.
Estructura de la amilina.
No obstante, esta estructura tiene una particularidad que puede ser potencialmente peligrosa: tiene cierta tendencia a formar agregados tóxicos para la célula. Más adelante hablaremos sobre cómo se las ingeniaron los científicos de Novo Nordisk para solventar este problema.
Funciones de la amilina
La acción de la amilina está encaminada a potenciar la acción de la insulina para regular los niveles de glucosa mediante 3 vías:
- Supresión del apetito, mediante su acción en regiones del sistema nervioso central que controlan el hambre y la saciedad. (Hay evidencias de la presencia de receptores de amilina en el área postrema, el hipotálamo, el núcleo accumbens, la amígdala y el núcleo del tracto solitario. Curiosamente, muchas de estas regiones están también implicadas en el control del movimiento y las emociones).
- Ralentización del vaciado gástrico, lo que disminuye la absorción de glucosa en el intestino. Se cree que los receptores de amilina ubicados en el sistema nervioso central estimulan al nervio vago para reducir los movimientos del estómago e incrementar el tiempo que pasan los alimentos en este órgano.
- Supresión de la secreción de glucagón, lo que reduce la síntesis de glucosa.
La amilina se almacena en vesículas de secreción junto con la insulina y ambas se co-secretan a la vez cuando se incrementan los niveles de glucosa en sangre.
Estas funciones convierten a la amilina en un candidato muy interesante para tratamientos contra el sobrepeso y la obesidad. De hecho, la pramlintida fue una primera versión modificada de la amilina aprobada en 2005 para el tratamiento de la diabetes.
Mecanismo de acción de la amilina
La amilina es reconocida por los receptores de amilina 1,2 y 3 (AMYR), una serie de receptores de tipo GPCR (hablé sobre los receptores GPCR aquí).
Los receptores de Amilina
Los receptores de amilina son un caso particular de GPCRs, ya que están formados por dos proteínas.
En primer lugar, tenemos el receptor de la calcitonina (CTR), una hormona con funciones en la homeostasis del calcio. Este receptor es un GPCR normal y corriente, que reconoce a la calcitonina cuando esta está presente y transmite señales al interior celular.
Estructura del receptor de calcitonina (violeta) unido a una proteína G (amarillo-verde). PDB:7TYO.
Sin embargo, este receptor tiene poca afinidad por la amilina. Su ligando natural es la calcitonina, para quien tiene una afinidad mucho superior. Para incrementar la afinidad del CTR por la amilina necesitamos de una segunda proteína (o familia de proteínas): las proteínas modificadoras de actividad del receptor (RAMP1,2, y 3 por sus siglas en inglés).
La unión de las RAMP al CTR fuerza un cambio en la conformación del CTR que incrementa entre 20 y 30 veces la afinidad de este receptor por la amilina. De esta manera, la combinación de CTR con las RAMP genera 3 receptores de amilina (AMYR) funcionales:
- AMY₁R: CTR + RAMP1
- AMY₂R: CTR + RAMP2
- AMY₃R: CTR + RAMP3
Estructura de los receptores de amilina (CTR+RAMP). Fuente
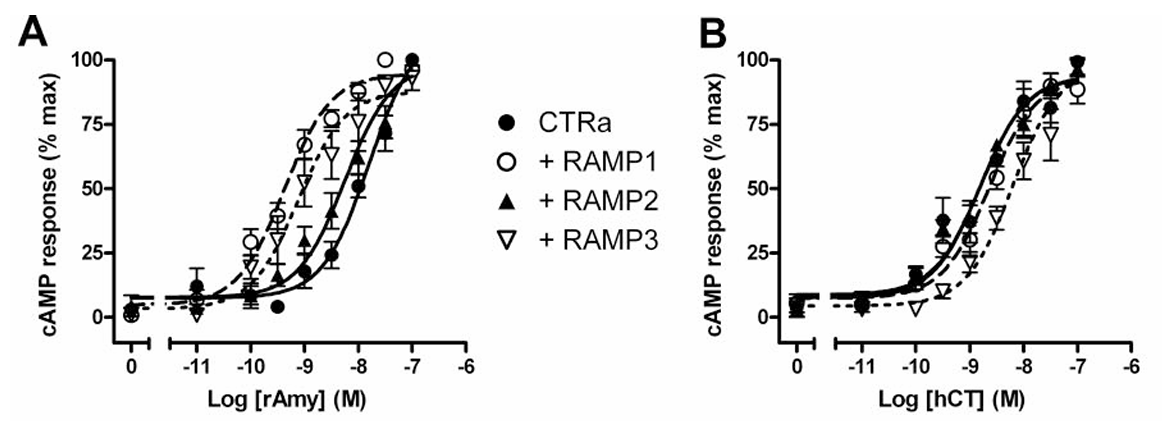
El siguiente experimento de un estudio de 2008 nos da evidencia de ello:
En la imagen se observan dos curvas de dosis-respuesta. Se emplean para conocer cómo afecta un fármaco a la actividad de un receptor. En este caso, medimos la activación del receptor por la concentración de AMPc (la molécula que se produce cuando se activa el receptor, en el eje Y) en función de cuanto ligando del receptor hay en el medio (eje X). De manera lógica, a mayor concentración de ligando, más actividad del receptor.
A la izquierda se mide la activación del receptor CTR en solitario o en combinación con cada uno de las RAMPs en función de la concentración de amilina. El resultado muestra que el receptor CTR aislado tiene menor afinidad por la amilina que cuando el CTR está asociado a RAMP1 o 3. Explicación: los niveles de AMPc se elevan a concentraciones más altas de amylina cuando el CTR está solo (puntos negros). En cambio, cuando está también presente RAMP1 (círculo blanco) o RAMP3 (triángulo blanco), se necesita menos concentración de amilina para conseguir una señal de AMPc. Como el receptor CTR+RAMP1/3 es más afín a la amilina, se observa un efecto ya desde dosis de amilina más bajas, y la curva despega antes.
En cambio, a la derecha se observa el efecto cuando en vez de amilina, echamos calcitonina al medio (el ligando natural del CTR). El efecto es el contratio: el CTR tiene mucha más afinidad por la calcitonina que los receptores de amilina.
De esta manera, la afinidad del CTR por la amilina se incrementa más de 25 veces cuando está presente alguna de las RAMP, sobre todo RAMP1 o 3. El AMYR tiene una alta afinidad por amilina, pero es interesante observar que el CTR por sí solo también tiene algo de afinidad por la amilina y puede activarse en su presencia. Será interesante tener esto en cuenta a la hora de evaluar los posibles efectos secundarios que tenga un análogo de la amilina.
Los problemas de la amilina
Aparte de los problemas gastrointestinales comunes a este tipo de terapias, existen varios problemas asociados al uso de la amilina o posibles análogos como terapia.
En primer lugar, la amilina tiene cierta tendencia a agregarse y formar precipitados insolubles tóxicos para la célula, que termina muriendo. Este proceso patológico ocurre en las islas de Langerhans del páncreas en pacientes de diabetes tipo 2 y contribuye a la disfunción pancreática y la progresión de la enfermedad. Esto supone un problema a la hora de administrar un posible fármaco con grandes dosis de amilina, ya que podría ser tóxico para el tejido.
En segundo lugar, la amilina es reconocida con mayor afinidad por los receptores de amilina, pero el receptor de calcitonina sigue teniendo cierta afinidad por este péptido. Resulta necesario diseñar un compuesto con alta especificidad por los receptores de amilina para evitar efectos secundarios asociados a la activación del receptor de calcitonina.
Por último, el tiempo de vida media de la amilina es de solo 20 minutos. Sumado a la necesidad de administrarla mediante inyecciones para evitar el sistema digestivo, sería muy complicado y tedioso para el paciente tener que seguir esta pauta de administración. De hecho, la pramlintida debía inyectarse tras cada comida, 3 veces al día.
Estos problemas, que no son pocos, son los que tuvo que tratar de solucionar el equipo de Novo Nordisk para conseguir un fármaco eficaz y seguro.
Cagrilintida
Desarrollo de la cagrilintida
¿Problemas con la amilina? Vamos a solventarlos uno a uno.
Formación de agregados tóxicos
Resulta que la secuencia de aminoácidos de la amilina humana tiene cierta tendencia a agregarse. Los fenómenos de agregación proteicos ocurren cuando las proteínas pierden su estructura normal y se vuelven “pegajosas”, en el sentido de que se unen a otras proteínas a las que normalmente no se unirían. Esta agregación provoca que las proteínas pierden su estructura (y, por tanto, su función), lo que resulta tóxico para la célula. De hecho, varias enfermedades neurodegenerativas como el Alzheimer presentan este mismo problema. En la diabetes, se ha osbervado que la propia disfunción de las células del páncreas se debe a la acumulación tóxica de agregados de amilina, lo que contribuye a la patología.
Ahora imaginemos una inyección de amilina. La gran concentración de amilina presente en la zona de inyección podría resultar muy dañina para el tejido donde se inyecte. Por suerte, este mismo problema ya surgió al idear la pramlintida. Para solventarlo, la estructura de la pramlintida está basada a su vez en la amilina de la rata, que no tiene esta tendencia a formar agregados tóxicos porque algunos de sus aminoácidos son distintos.
Por tanto, los científicos de Novo Nordisk se basaron en la estructura de la pramlintida. En la imagen se observan en rojo los aminoácidos mutados respecto a la amilina humana (h-amylin). Nótese que muchos de los aminoácidos sustituidos coinciden con los presentes en la amilina de rata y en la pramlintida:

La prolina (P), un aminoácido particular
Esta parte es pura elucubración mía. Me estaba fijando en los aminoácidos modificados que presentaba la cagrilintida, y me resultó curioso ver que muchos de los cambios correspondían con el aminoácido prolina (P).
¿Por qué emplear este aminoácido para reducir la agregación?
La prolina es un aminoácido un tanto peculiar. Es un aminoácido en tanto que contiene un grupo amino () y un grupo carboxilo (), pero también contiene un anillo de carbonos poco común.
El resultado de este anillo es que los enlaces que unen los átomos de la prolina son más rígidos y tienen menos capacidad de moverse libremente. Esto me lleva a pensar que la alta cantidad de prolinas que contiene la pramlintida tiene como función dotar a la molécula de una estructura más rígida. El poco grado de movimiento que tienen las prolinas “fuerzan” a que la molécula de pramlintida tenga una estructura más estable, con menos tendencia a la agregación. Y todo ello, sin afectar a su sensibilidad por el receptor de amilina.
Aumento de la vida media
El tiempo de vida medio de la amilina es de 20 minutos. Para poder incrementar su vida útil, se decidió probar a lipidar la molécula como ya se había hecho con éxito en la liraglutida y la semaglutida.
Mediante la modificación de algunos aminoácidos por Lisinas (K) y su posterior lipidación, se consiguió incrementar la vida media del compuesto hasta ~1 semana sin una pérdida significativa de afinidad por el receptor de amilina.
Los últimos retoques
Por último, gracias a la experiencia de Novo Nordisk en el desarrollo de péptidos bioactivos, una serie de pruebas extra permitieron mejorar las propiedades farmacocinéticas de la amilina:
- Introducción de un glutamato (E) y una arginina (R) en la región central de la estructura. La carga negativa del glutamato forma un puente salino con la positiva de la arginina, lo que dota a la estructura de una mayor rigidez y estabilidad.
- Mantenimiento del puente disulfuro entre dos cisteinas (C) en la región N-terminal para mantener la estabilidad.
- Finalmente, mantenimiento de la amidación en el extremo C-terminal para no perder potencia de reconocimiento del receptor.
Con todos estos cambios finalmente obtenemos la Cagrilintida, un análogo de la amilina de larga duración con una gran selectividad hacia el receptor de amilina.
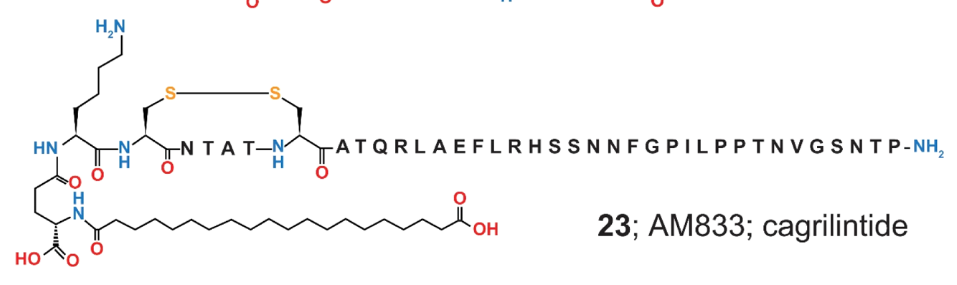
En la siguiente imagen se puede observar la estructura de la cagrilintida embebida dentro del bolsillo de unión del receptor de la amilina. A la derecha, se aprecian los cambios comentados anteriormente:
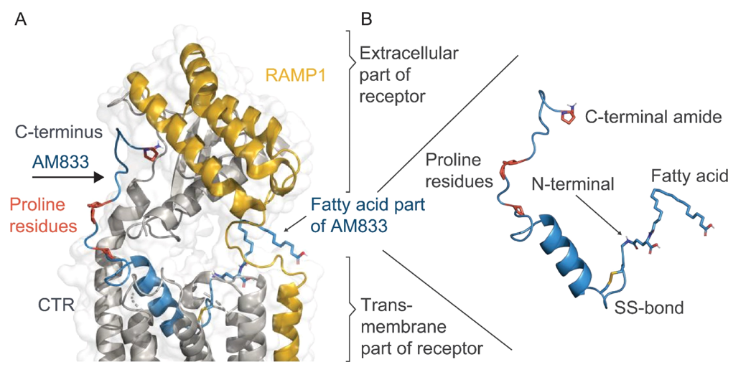
Eficacia de la cagrilintida
La fase de jugar con la estructura del fármaco para mejorar sus propiedades fisicoquímicas es muy entretenida. Pero la realidad es que, tras todos estos cambios, el fármaco debe ser eficaz y seguro.
¿Qué tal se comporta la cagrilintida?
En ensayos con ratas, la administración subcutánea de concentraciones crecientes de cagrilintida (cuanto más oscuro el azul, más dosis) provoca una reducción en la ingesta de comida.
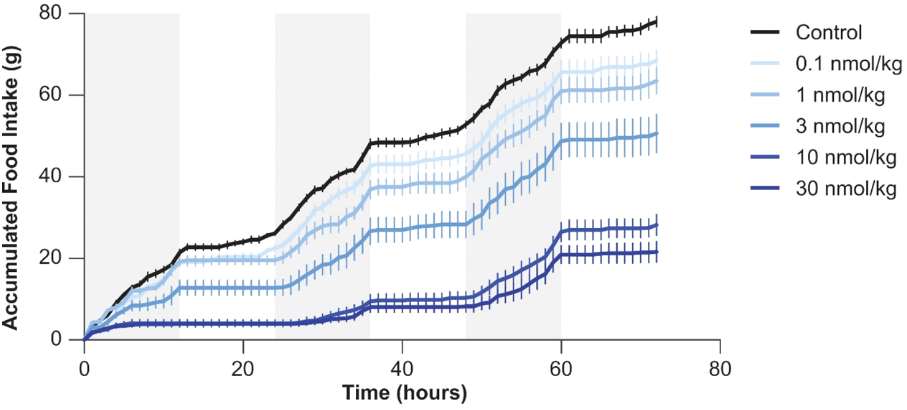
A nivel sanguíneo, la administración de una única dosis de cagrilintida en ratas consigue una elevación de los niveles del fármaco que disminuye lentamente a lo largo de los días.
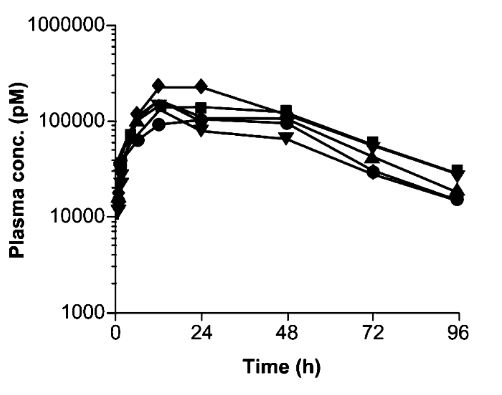
¿Y qué nos dicen los ensayos en humanos?
Un primer ensayo de fase 2 (NCT03856047) probó el efecto de diferentes dosis de Cagrilintida para inducir pérdida de peso en adultos con sobrepeso u obesidad durante 26 semanas. Como control, se empleó un grupo placebo y otro al que se administró Liraglutida.
Los resultados mostraron que la administración semanal de 2,4 mg de cagrilintida provocaba una pérdida de peso superior a la liraglutida al cabo de 26 semanas:
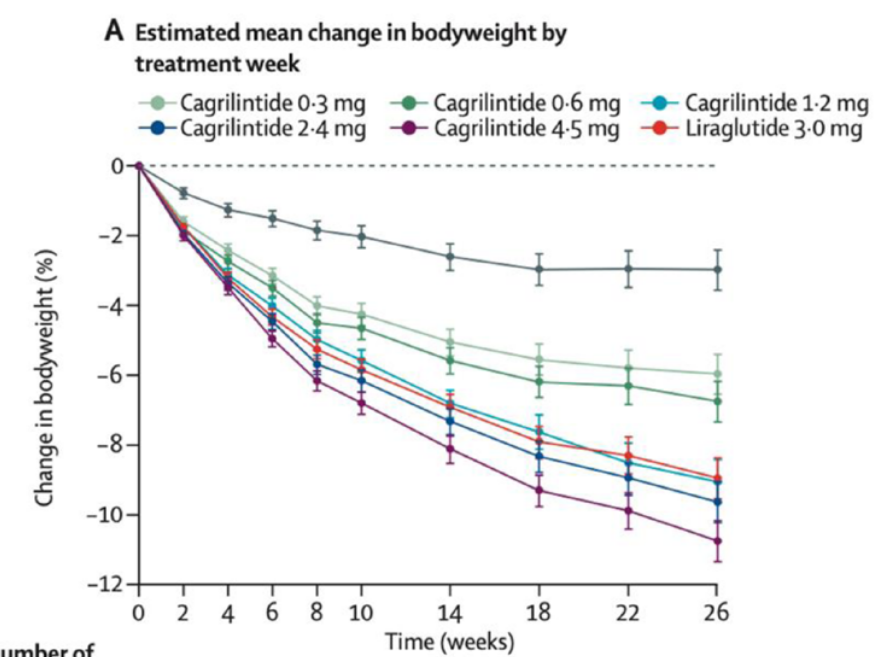
Además, en este estudio se observó que los pacientes con cagrilintida continuaban perdiendo peso pasadas las 26 semanas. Los efectos adversos fueron en línea con los ocasionados por este tipo de tratamientos, con un 40-60% de pacientes reportando efectos secundarios vs el 30 % de los pacientes con placebo. Estos datos iniciales apuntaban a que el uso de la cagrilintida podía ser prometedor en humanos.
No obstante, esta pérdida de peso no parecía ser nada del otro mundo. Recordemos que la semaglutida por sí sola ya produce una pérdida de peso del 15 %.
¿Por qué continuar entonces con su desarrollo?
Porque lo relevante de la cagrilintida no es que haga perder peso a los pacientes, sino que lo hace por mecanismos distintos a los de la semaglutida y demás análogos de GLP-1. Esto quiere decir que quizás, combinando ambos fármacos, podríamos conseguir potenciar dos rutas distintas con el mismo efecto final: perder peso.
Eficacia de CagriSema
Hechas las presentaciones, es momento de ver qué tal se está comportando este fármaco en la realidad. Veamos los resultados de los ensayos clínicos hasta la fecha.
Un primer ensayo de fase 1b (NCT03600480) probó la combinación de 2,4 mg de semaglutida y dosis crecientes de cagrilintida en individuos con sobrepeso u obesidad. Estos ensayos suelen estar enfocados a entender la farmacocinética, farmacodinámica y seguridad del compuesto, y suelen realizarse en individuos sanos. No obstante, en este caso se incluyeron individuos con sobrepeso, por lo que pudimos tener un primer acercamiento a la eficacia de CagriSema.
La pauta de administración fue la siguiente: cada paciente se asignó a un grupo, se le administraron dosis crecientes del fármaco durante 16 semanas hasta llegar a su dosis límite, se mantuvo esa dosis durante otras 4 semanas, y finalmente se retiró el fármaco y se vio su evolución durante 5 semanas. Los pacientes en el grupo “placebo” recibieron únicamente dosis de 2,4 mg de semaglutida.
Los resultados del ensayo mostraron que dosis de cagrilintida > 1,2 mg + 2,4 mg de semaglutida parecían producir una pérdida de peso superior a la de la semaglutida por sí sola.
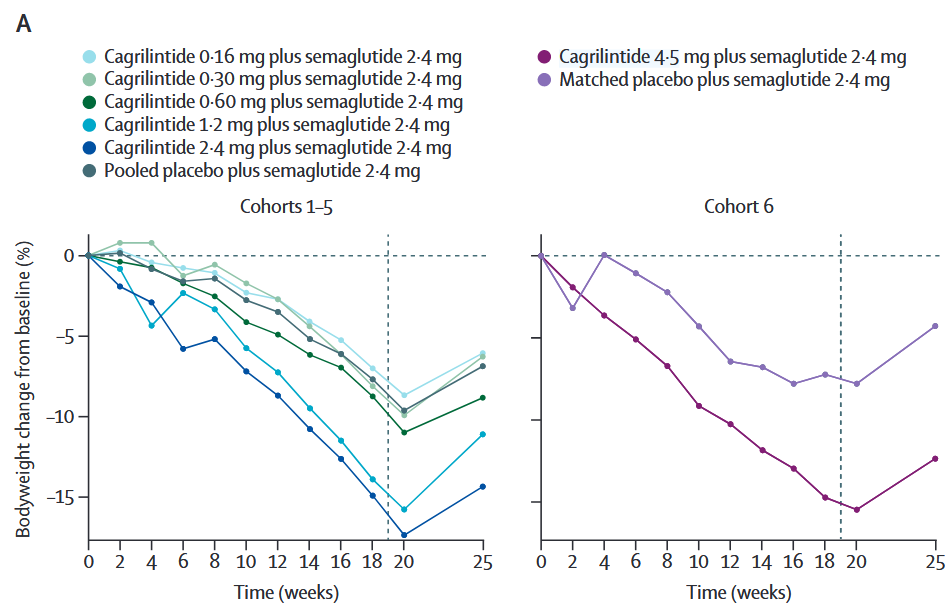
Los datos también mostraron que parecía haber un máximo en términos de pérdida de peso: la bajada era máxima (-17 %) con dosis de 2,4 mg de cagrilintida, mientras que una dosis superior no se traducía necesariamente en pérdidas de peso más pronunciadas.
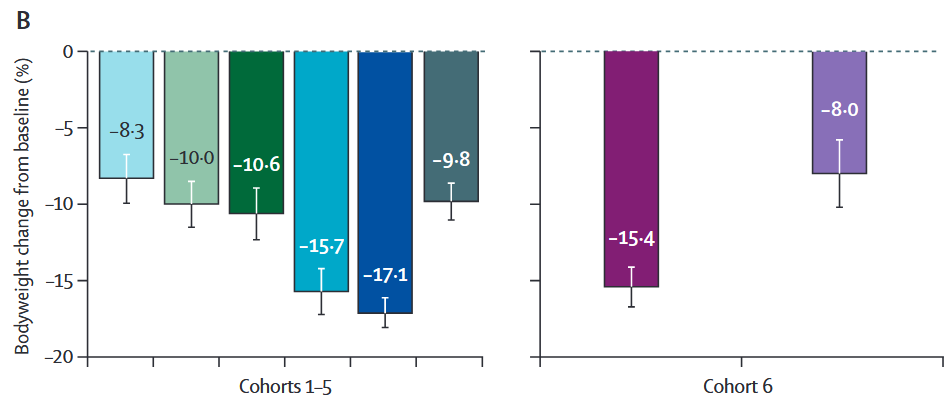
Precisamente la dosis de 2,4 mg resultó ser la elegida para continuar los ensayos clínicos porque tenía la combinación óptima de eficacia, tolerabilidad y seguridad. No tendría ningún sentido aumentar la dosis por encima de ese nivel cuando la eficacia no mejora pero sí empeoran los efectos secundarios.
Otros hechos no menos importantes que constató este ensayo fueron:.
- La combinación de cagrilintida y semaglutia tenía efectos sinergísticos para la pérdida de peso.
- El fármaco era generalmente bien tolerado y no existían interacciones entre ambos fármacos.
Pasamos ahora a ver los resultados del ensayo de fase 3 REDEFINE 1 (NCT05567796), en el que se evaluó la eficacia de CagriSema vs cagrilintida, semaglutida o placebo por separado. En este caso, el estudio empleó a 2108 adultos con obesidad o sobrepeso con alguna complicación relacionada con la obesidad.
Los resultados nos indican que la combinación de CagriSema tiene unos efectos más potentes que los fármacos por separado, consiguiendo una reducción de peso media del 20,4 % respecto al 3 % conseguido con el placebo. CagriSema también provoca pérdidas de peso superiores a las de los tratamientos por separado, lo cual confirma lo ya observado anteriormente.
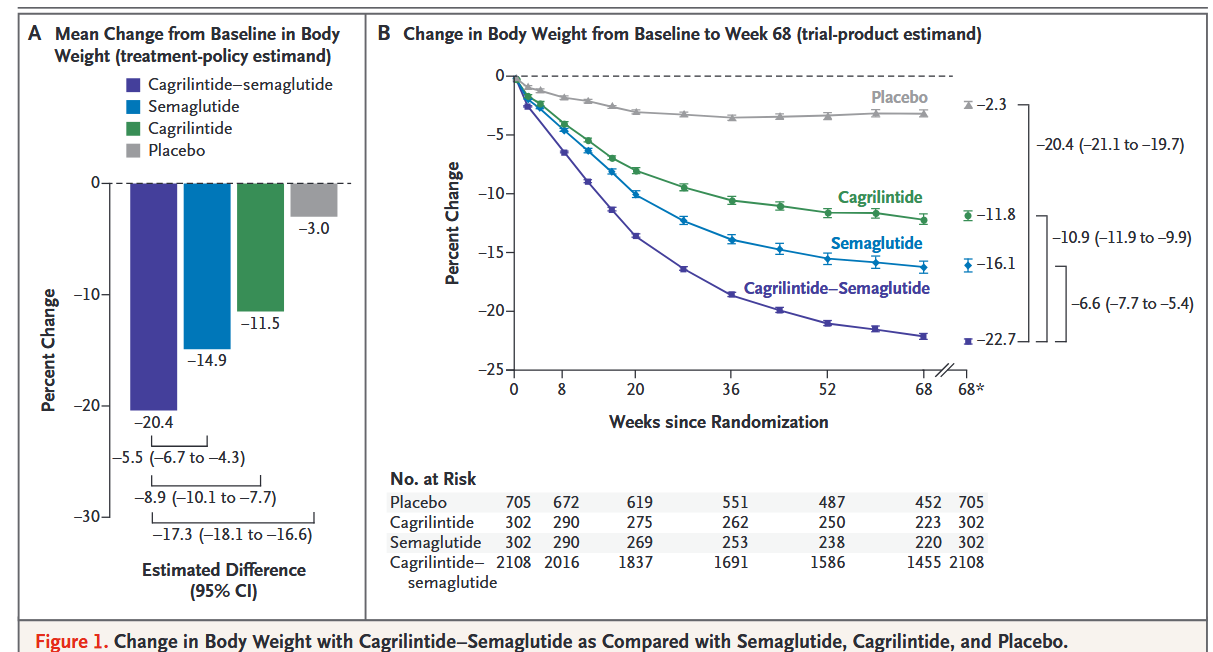
Sin embargo, estos resultados no parecieron gustar al mercado, que quizás esperaban ver que CagriSema tenía un efecto superior que la tirzepatida de Lilly (que logra una pérdida de peso del 22 % a dosis más altas). Las acciones de Novo Nordisk cayeron un 20% cuando se publicó este estudio.
Ya comenté en redes lo que me parecía la opinión del mercado respecto a los resultados. En mi opinión, los datos del ensayo son buenos y alentadores por varios motivos:
- El fármaco es eficaz y tolerable en dosis prolongadas.
- La pérdida de peso es del 20,4 %, lo cual no es nada desdeñable teniendo en cuenta que la tirzepatida de Lilly necesita de 15 mg de producto para conseguir ese nivel de pérdida de peso. El argumento de que lo importante es maximizar la pérdida de peso es cortoplacista y no se sostiene por ningún lado.
- El ensayo permitía una pauta de administración variable, es decir, que los médicos podían elegir no aumentar más la dosis al paciente si los efectos observados ya eran lo suficientemente buenos. De hecho, solo el 56 % de los pacientes alcanzó la dosis máxima recomendada.
- El ensayo terminó a las 68 semanas, pero eso no quiere decir que el fármaco deje de hacer perder peso a los pacientes. Si bien es cierto que la mayor pérdida de peso ocurre en etapas tempranas, se puede seguir perdiendo peso en etapas más tardías del tratamiento.
- Finalmente y en relación de nuevo a la tirzepatida, es cuanto menos osado hacer una comparativa de pérdida de peso entre dos fármacos que no se han analizado a la vez. Las variables cambian (participantes, lugares de realización del ensayo, pautas de administración, duración, etc) y eso afecta a los resultados. De hecho, el 22 % de pérdida de peso que provoca la tirzepatida es a las 72 semanas, mientras que este ensayo sólo llegó a las 68. Tendremos que esperar a los resultados del ensayo REDEFINE 4 que sí compara cara a cara ambos fármacos.
Por su parte, el ensayo REDEFINE 2, enfocado a pacientes con diabetes además de sobrepeso, resultó también arrojar resultados positivos, con una pérdida de peso media del 15,7 % a las 68 semanas. Puede parecer poco, pero tengamos en cuenta que en este ensayo la pérdida de peso no es el objetivo, sino el control de la glucemia.
En conjunto, los datos respecto a la eficacia de CagriSema son alentadores. El problema es que quizás esto no sea suficiente.
Expectativas de comercialización de CagriSema
A pesar de que CagriSema haya demostrado potencia y eficacia para la pérdida de peso, dista mucho de estar a las puertas del éxito. Cuando la semaglutida vio la luz, estaba todo por hacer. Novo Nordisk se encontró un mercado en auge carente de péptidos activos con tal nivel de eficacia para controlar la diabetes y el sobrepeso.
Pero con CagriSema esto no es así.
Ahora mismo, el mercado es muy competitivo. Muchas compañías han entrado pisando fuerte en este sector, con fármacos muy potentes. Y el problema es que CagriSema no representa un cambio de paradigma.
Sí, el fármaco hace perder un 20 % de peso, que no es nada desdeñable. Pero es que la tirzepatida de Lilly ya consigue eso. Y, a diferencia de CagriSema, la tirzepatida ya está siendo comercializada y capturando cuota de mercado, mientras que las mejores expectativas apuntan a que la comercialización de CagriSema llegará para finales de 2026.
Por supuesto, no todo es la potencia en cuanto a pérdida de peso se refiere. Aprobación por los organismos reguladores, manufactura y distribución, aceptación por las aseguradoras, protección de las patentes, … todo cuenta a la hora de proyectar las ventas que generará CagriSema. Lo más seguro es que reciba la aprobación y se comercialice sin problemas. Pero tenemos que entender que parte desde una situación de desventaja cuando ya existe una alternativa en el mercado.
En mi opinión, podemos ver a CagriSema como una estrategia defensiva que ayude a Novo Nordisk a mantener su posición en el mercado cuando expiren las patentes de la semaglutida, pero no como un catalizador que transforme el ecosistema. Quizás el compuesto no “supere” en términos de potencia a la tirzepatida de Lilly, pero desde luego que la iguala. Y recordemos que no estamos en un mercado en el que the winner takes it all. Novo Nordisk está en un mercado en crecimiento y, si bien este compuesto no supone una revolución tecnológica, le permitirá asegurarse un asiento en el tren de la diabetes y la obesidad.
Seguiremos pendientes del desarrollo de CagriSema.
Referencias
@KruseEtAl_2021_DevelopmentCagrilintideLongActing @LauEtAl_2021_OnceweeklyCagrilintideWeight @GarveyEtAl_2025_CoadministeredCagrilintideSemaglutide