El camino de la innovación farmacéutica rara vez ofrece apuestas seguras, pero VK2735 está acumulando razones para atraer la mirada de los inversores más exigentes.
Introducción
El compuesto VK2735 es un péptido análogo deGLP-1/GIP que está siendo desarrollado para tratar trastornos metabólicos como obesidad, diabetes e hígado graso.
La estructura exacta de VK2735 es confidencial. Existe una patente concedida a finales de 2023 a nombre de VKTX (Nº: 11744873) que protege a varios péptidos análogos de GLP-1/GIP 1. Un vistazo a la patente nos indica que, probablemente, el compuesto se trata de un derivado de la siguiente estructura:
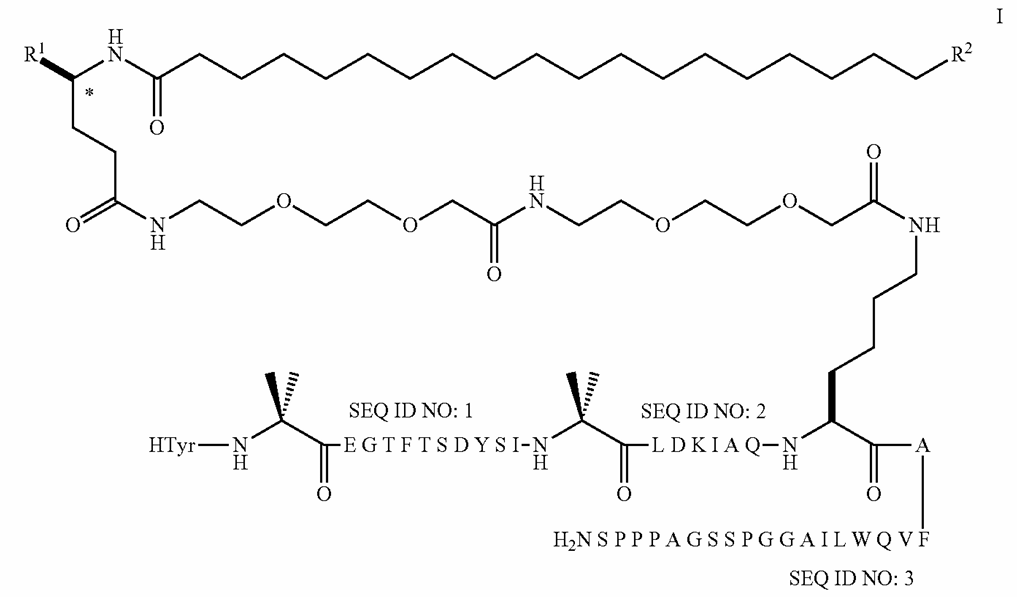 Péptido base que cubre la patente de VKTX.
Péptido base que cubre la patente de VKTX.
La molécula parece un péptido al estilo de los desarrollados por Novo Nordisk o Eli Lilly, con una secuencia lineal de aminoácidos de cuyo centro emana un ácido graso para incrementar su vida media. Sin embargo, con estos datos no podemos extraer muchas conclusiones ni estudiar en profundidad la relación entre la estructura del péptido y su actividad biológica. Vamos directamente con la evidencia en estudios animales.
Ciencia
Evidencia preclínica
La evidencia preclínica que respalda a VK2735 es escasa y se reduce a dos presentaciones de póster en un congreso y otra corporativa. En ellas se describe la eficacia del compuesto para reducir el peso y mejorar diversos marcadores metabólicos en un modelo de ratón obeso (Diet-induced obese mice, DIO mice)2.
En la primera presentación se abordó el efecto de VK2735 para mejorar diversos parámetros de obesidad. La administración diaria de VK2735 en ratones obesos produjo una reducción transitoria de la ingesta de alimentos que se correspondía con una disminución del 26 % en el peso corporal en apenas 10 días:
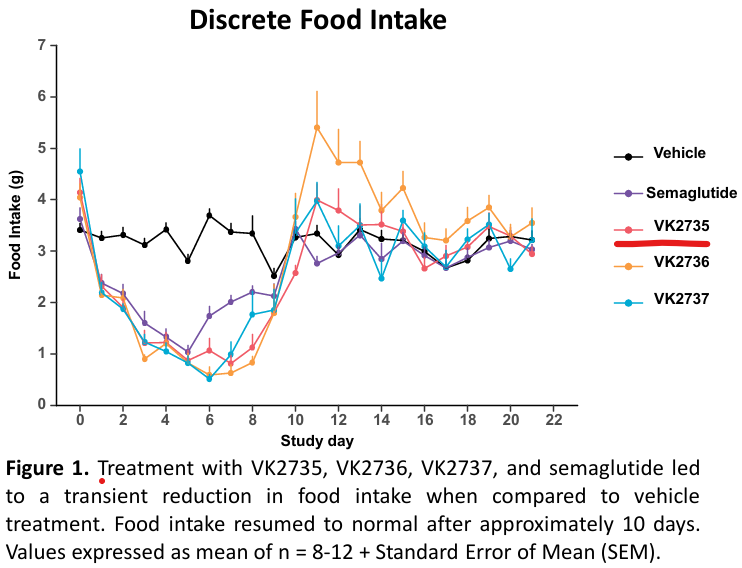
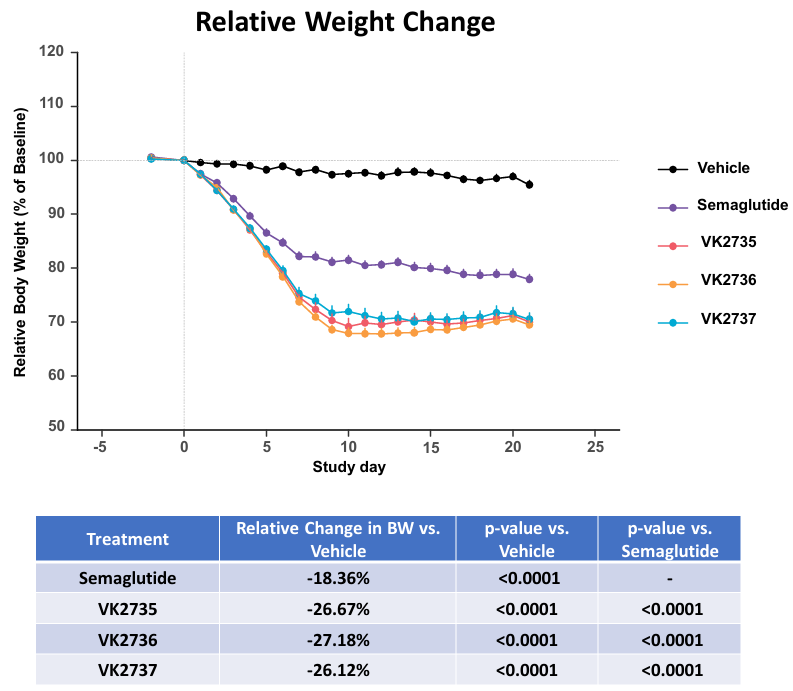
Como comparación, también se observa que la pérdida de peso lograda es superior a la de la semaglutida, lo que ya nos da indicios de su mayor eficacia. Un hecho curioso es que, pasados 10 días, el VK2735 deja de inducir mayor pérdida de peso, mientras que la semaglutida continúa reduciéndolo a lo largo de los días.
En el mismo estudio también se constató que VK2735 era capaz de mejorar los niveles de glucosa, insulina y lípidos en sangre a niveles similares a los de la semaglutida. Finalmente, se observó que también se reducía el índice de esteatosis (hígado graso) en los ratones tratados, aunque los valores eran similares a los alcanzados con la semaglutida:
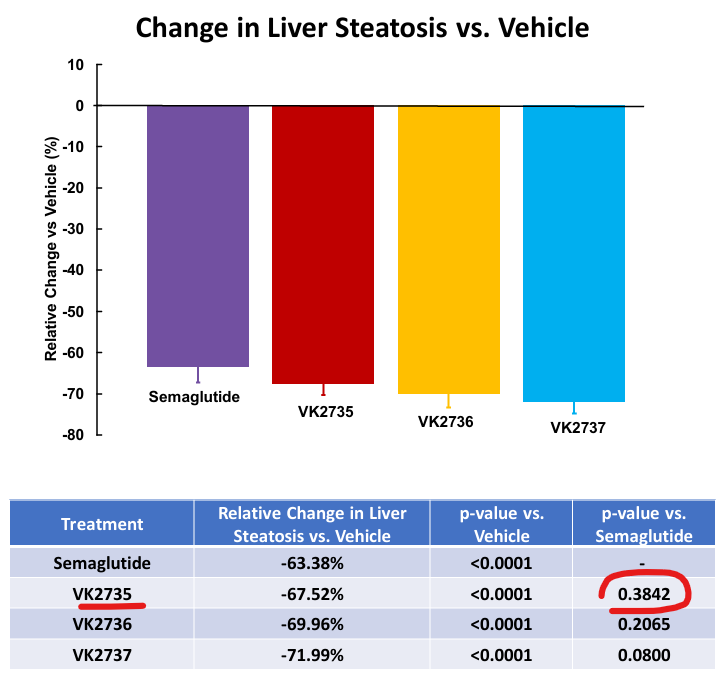
El medicamento parecía mejorar el perfil de la semaglutida en cuanto a pérdida de peso. Pero recordemos que VKTX no está compitiendo sólo con la semaglutida, pues el fármaco más potente actualmente en el mercado es la tirzepatida. Esto es precisamente lo que trató de abordar el segundo póster.
En este caso, el efecto de pérdida de peso provocado por VK2735 era idéntico al de la Tirzepatida:
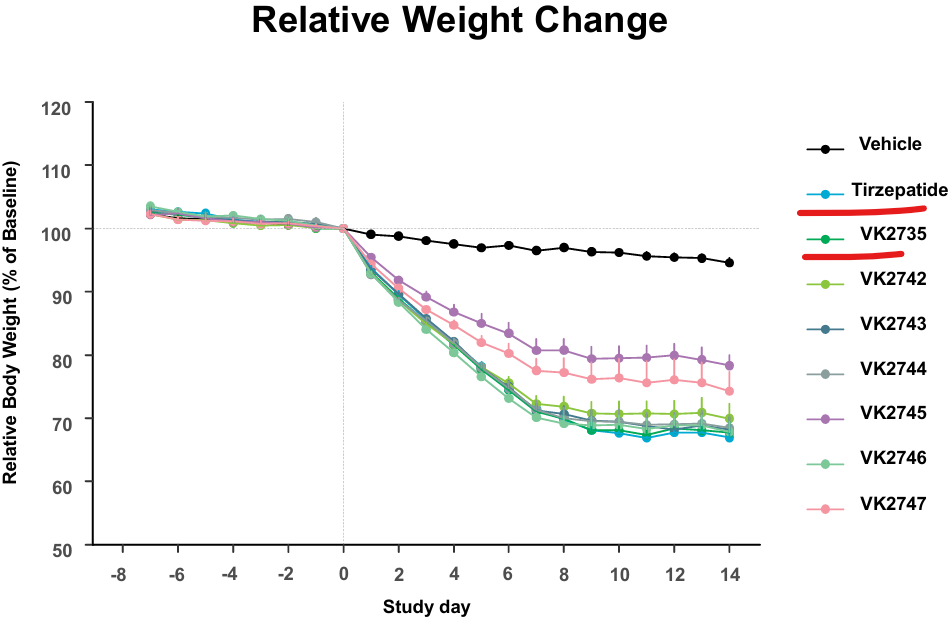
No obstante, en otros análisis de niveles de glucosa, triglicéridos y colesterol parece que la tirzepatida es ligeramente mejor que VK2735 (y digo ligeramente porque no se indican tests estadísticos que confirmen lo que se aprecia en las gráficas). Estos datos nos indican que el VK2735 es efectivo en ratones a un nivel comparable al de la tirzepatida, algo lógico dado que ambos atacan a los mismos receptores.
En otra presentación a inversores 3 se aportan algunos datos más:
En primer lugar, los compuestos de VKTX tendrían una afinidad < 500 nM por los GLP-1R y GIPR, lo cual sería similar a la tirzepatida o la retatrutida (recordemos que aquí, cuanto menor es al valor, mayor es la capacidad de unión).
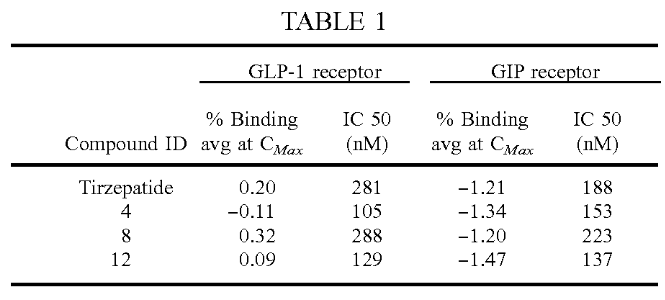 Extracto de la patente donde figuran compuestos entre los que se encuentra VK2735.
Extracto de la patente donde figuran compuestos entre los que se encuentra VK2735.
Segundo, un estudio en primates nos indica que el tiempo de vida medio del compuesto es variable, en torno a los 2-7 días. Pero no se indica ni de qué depende la variabilidad ni ningún dato adicional, cuando este dato podría ser crucial para identificar si podría administrarse diaria o semanalmente.
Todo esto me lleva a concluir que los datos preclínicos deberían ser tomados con cierto escepticismo: no conocemos el mecanismo de acción de VK2735, ni la relación de su estructura con su actividad, ni existen publicaciones oficiales en revistas revisadas por pares, ni estudios realizados por grupos independientes. La evidencia presentada tiene una fiabilidad limitada.
Evidencia clínica
Vía subcutánea
Ensayo fase 1 SAD/MAD (NCT05203237)
Este ensayo finalizó a finales de 2024 4 y se trató de un ensayo combinado de la seguridad y tolerabilidad de VK2735. También se incluyeron como objetivos secundarios la pérdida de peso y la mejora del perfil metabólico.
- Parte A: dosis única subcutánea
- Parte B: dosis semanal subcutánea durante 4 semanas.
- Parte C: dosis diaria oral durante 28 días.
Me llama la atención que en los criterios de inclusión del estudio no se especifica que el paciente deba tener sobrepeso u obesidad:
 Criterios de inclusión en el ensayo de fase 1.
Criterios de inclusión en el ensayo de fase 1.
No obstante, luego en los resultados nos muestran a pacientes con BMI > 30. ¿Dónde está el error?
De los resultados del ensayo podemos extraer algunas buenas conclusiones:
- El fármaco produce una pérdida de peso significativa, un 7,8 % en 4 semanas a las dosis más altas.
- La pérdida de peso es proporcional a la dosis empleada, con dosis mayores evocando una pérdida de peso superior.
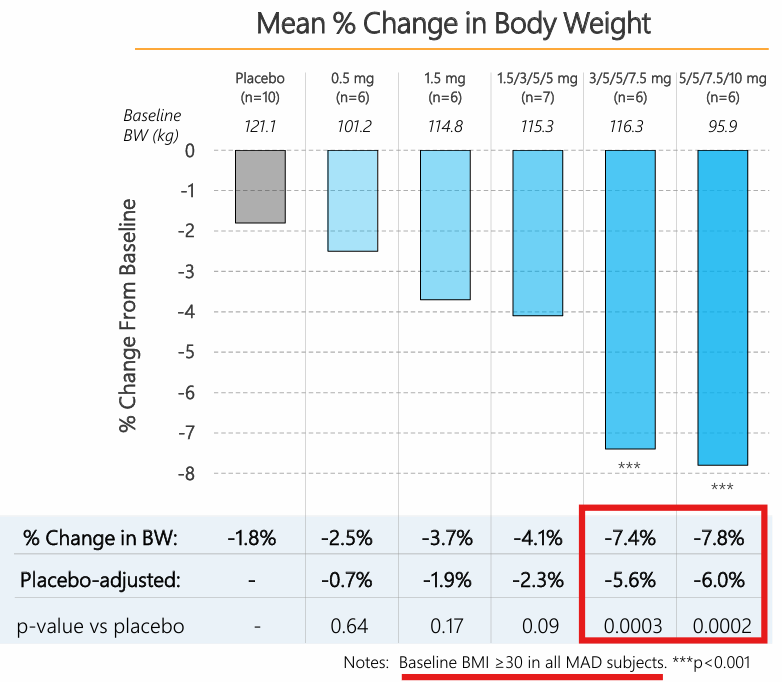
- No se vieron signos de que la pérdida de peso se fuera a detener al terminar las 4 semanas, lo que indica potencial de pérdidas de peso superiores.
- Los efectos secundarios fueron limitados y parecidos a los del grupo control. Tampoco se apreciaron efectos secundarios graves ni ningún paciente que tuviera que abandonar el ensayo a causa del tratamiento.
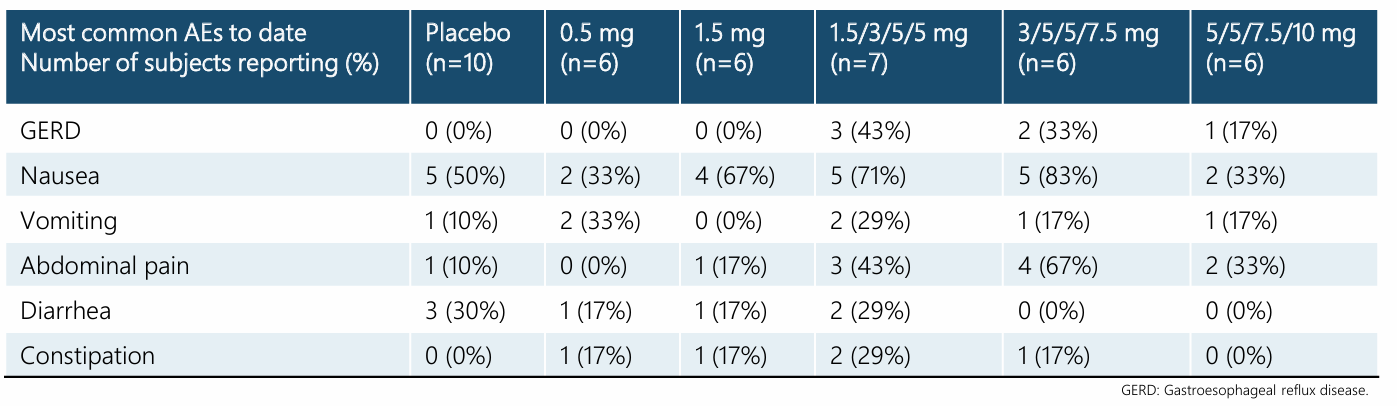
- Y, aunque no nos muestran más datos, nos indican que el perfil de farmacocinética apoya que la administración del fármaco sea semanal.
Ensayo fase 2 (NCT06068946)
Este ensayo se centró en estudiar la eficacia de VK2735 en la pérdida de peso 5.
| Diseño del estudio | |
|---|---|
| Fase | 2 |
| Pacientes | - Obesidad (BMI > 30) - Sobrepeso (BMI > 27) + afección relacionada |
| Ruta de administración | Subcutánea |
| Frecuencia | Semanal |
| Dosis | 2,5 - 15 mg |
| Duración | 13 semanas |
| Criterios de valoración | - Primario: pérdida de peso (%) - Secundario: proporción de sujetos que experimentan pérdidas de peso superiores al 5 y 10 % - Otros: Incidencia de efectos adversos |
 Cronograma con las fases del estudio.
Cronograma con las fases del estudio.
Los resultados mostraron que la administración de VK2735 producía una pérdida de peso sustancial a las 13 semanas directamente proporcional a la cantidad de dosis administrada:
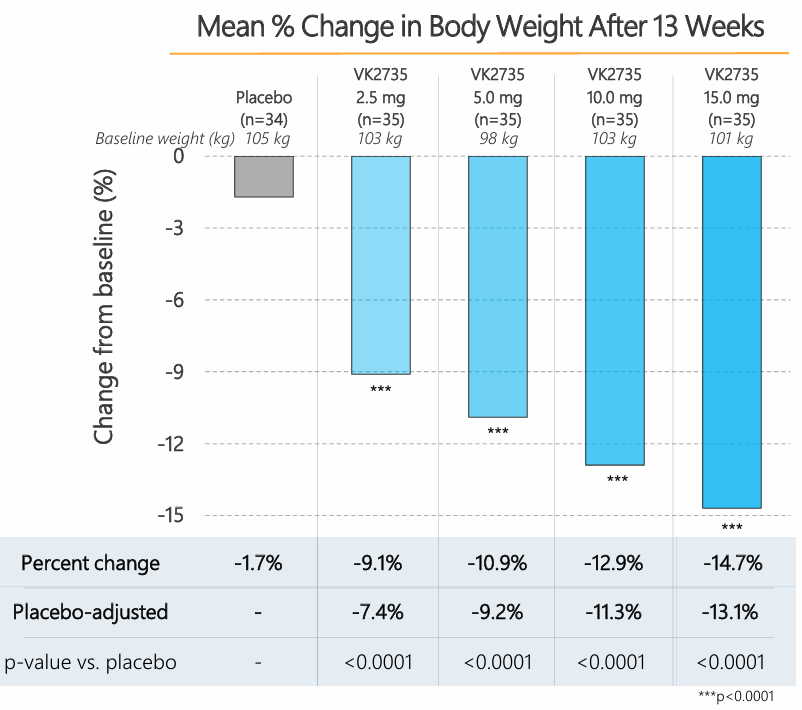
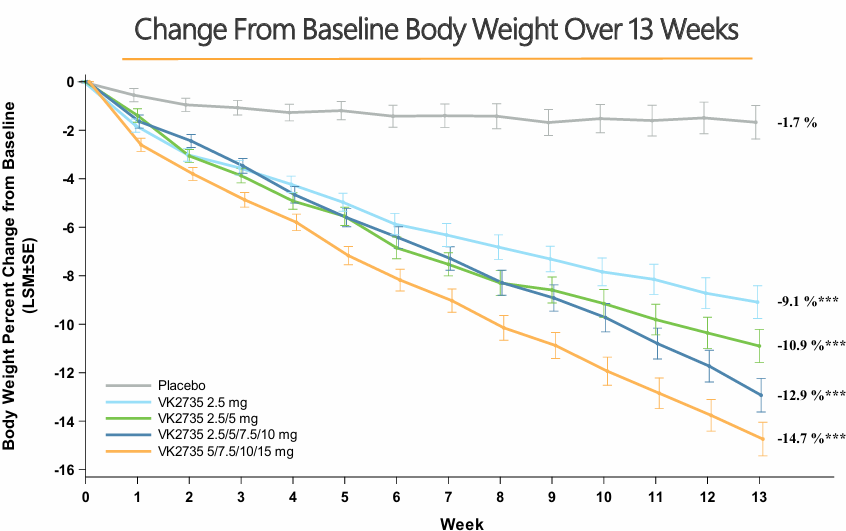
Además, se realizó un seguimiento durante un mes tras la administración de la última dosis, con el fin de conocer si los pacientes mantendrían la pérdida de peso. Los datos mostraron que el 83 % de los pacientes había mantenido su peso tras este mes, lo que podría sugerir que el fármaco es de actuación larga y podría administrarse mensualmente. Sin embargo, este último dato no tiene demasiado peso. Para saber si el fármaco se puede administrar mensualmente, habría que conocer la farmacodinámica del compuesto y si se mantiene a una concentración biológicamente relevante a estos tiempos tan largos.
Por último, un 80 % de los pacientes con prediabetes vieron normalizados sus niveles de azúcar en sangre tras el tratamiento, lo que podría permitir su uso en esta enfermedad.
A nivel de efectos secundarios, y como suele ser habitual en este tipo de fármacos, el VK2735 pareció ser generalmente bien tolerado, con la mayoría de efectos secundarios siendo de carácter leve o moderado. La aparición de efectos adversos se acumuló en las primeras semanas de tratamiento, lo que sugiere que quizás se podrían reducir ajustando el incremento de las dosis.
Los datos de pérdida de peso parecerían indicar que el VK2735 produce una pérdida de peso superior a la tirzepatida. No obstante, un usuario de Twitter ha señalado algo importante respecto a las dosis de VK2735 y la relación entre eficacia y seguridad (todo el crédito de lo siguiente es suyo).
Estos son los efectos adversos gastrointestinales que producen dosis comparables de VK2735 y de tirzepatida. Los datos son del ensayo de fase 2 de VK2735 vs el ensayo de fase 3 de tirzepatida para pacientes con obesidad:
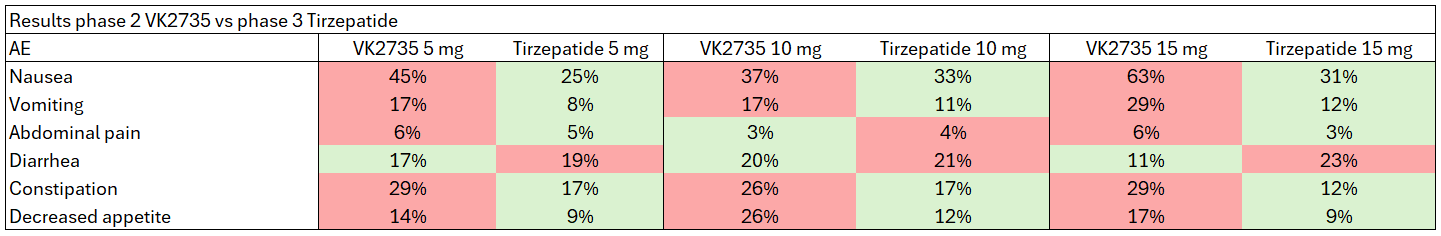
Si nos fijamos, veremos que la tirzepatida parece ser más segura que VK2735 a dosis equivalentes. De hecho, si tratáramos de ajustar por seguridad, nos encontraríamos con que la dosis equivalente a 15 mg de tirzepatida sería la de 2,5 mg de VK2735:
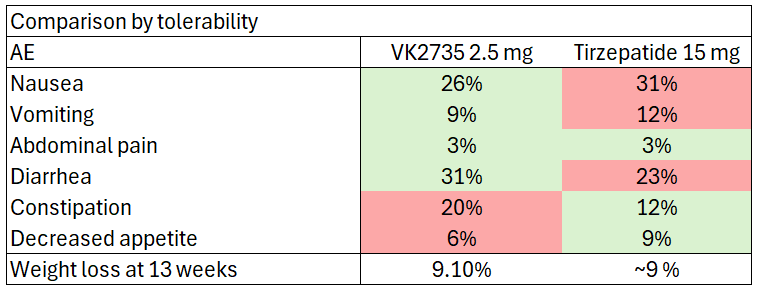
A estas dosis, los efectos secundarios que producen ambos fármacos son muy similares, al igual que la pérdida de peso. ¿Significa esto entonces que VK2735 es más potente que la tirzepatida?
Sí, con un pero. Si atendemos a las pautas de administración de ambos fármacos, se observa:
- Los incrementos de dosis en los ensayos de tirzepatida se producían cada 4 semanas.
- En cambio, los incrementos de dosis con VK2735 ocurrían cada 3 semanas.
A lo largo de las semanas, esta diferencia se acumulaba y provoca que, para la semana 13, se estuviera administrando mucha más cantidad de VK2735 que de tirzepatida.
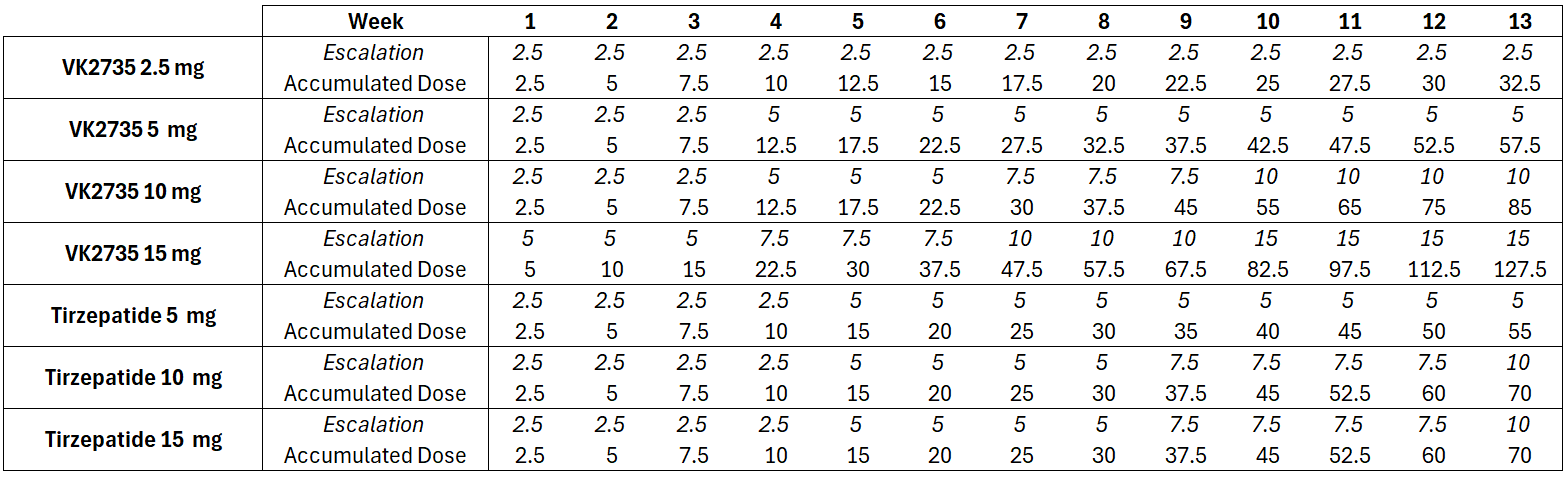
De esta manera, si sumamos ambos factores (que VK2735 parece ser algo más potente y que se administra más dosis) es como llegamos a la espectacular cifra de pérdida de peso que muestra VK2735. No es que VK2735 sea mucho más potente que la tirzepatida, sino que se administra mucha más dosis en el ensayo. De ahí que tanto la pérdida de peso como los efectos secundarios sean mucho más pronunciados con dosis totales equivalentes de ambos fármacos.
Este pequeño truco estaría ocultando la realidad: VK2735 y tirzepatida son moléculas mucho más similares de lo que podría parecer, porque su mecanismo de acción es el mismo y sus efectos son muy similares. Si acaso, lo que nos dice este ensayo es que el VK2735 podría ser algo más potente que la tirzepatida y permitiría a Viking Therapeutics manufacturar menos dosis de compuesto activo a más pacientes.
En cualquier caso, el fármaco ha entrado en ensayos de fase 3.
Vía oral
Ensayo fase 1 SAD/MAD (NCT05203237)
Mismo ensayo que el de la fase subcutánea, pero esta vez en su versión oral.
En este caso se probaron dosis de entre 2,5 y 100 mg administradas diariamente durante 28 días (o cada dos días en las dosis más altas). Los datos fueron igualmente buenos pasados los 28 días, tanto en seguridad como en pérdida de peso:
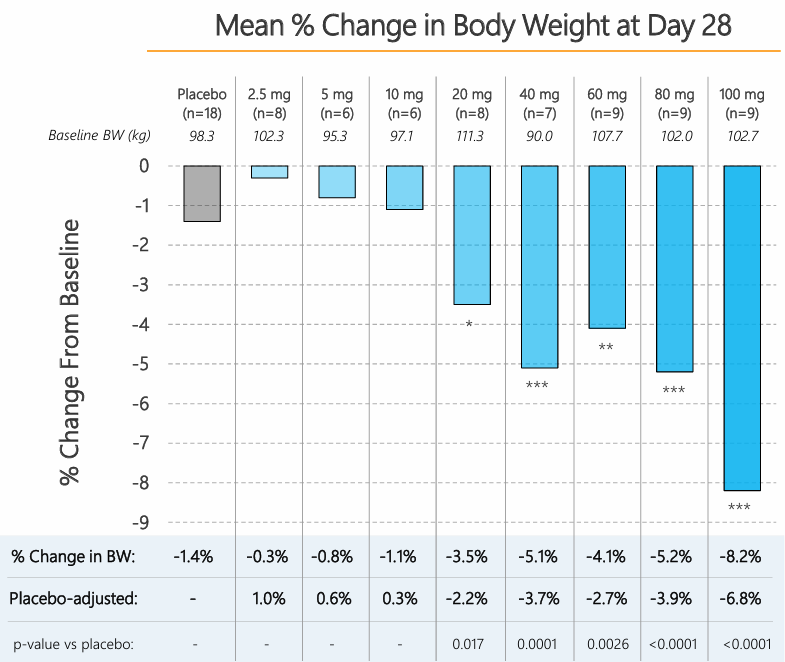
Además, los pacientes siguieron siendo monitorizados un mes después de recibir la última dosis y se observó que mantenían el peso perdido, lo que sugiere que el fármaco podría tener un efecto retardado o incluso que podría mantenerse a dosis más bajas durante periodos más largos.
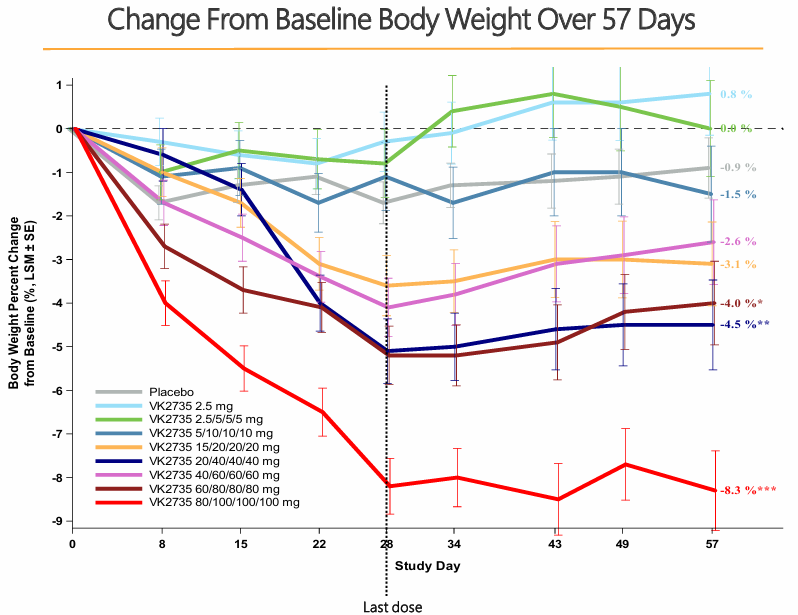
A los 15 días de comenzar el ensayo, un último subgrupo empezó a recibir el VK2735 cada dos días y se observó que a pesar de reducir la dosis, se seguía perdiendo peso. Esto sugiere la posible existencia de un punto de saturación donde no es necesario más fármaco y se puede reducir la dosis sin afectar a la pérdida de peso.
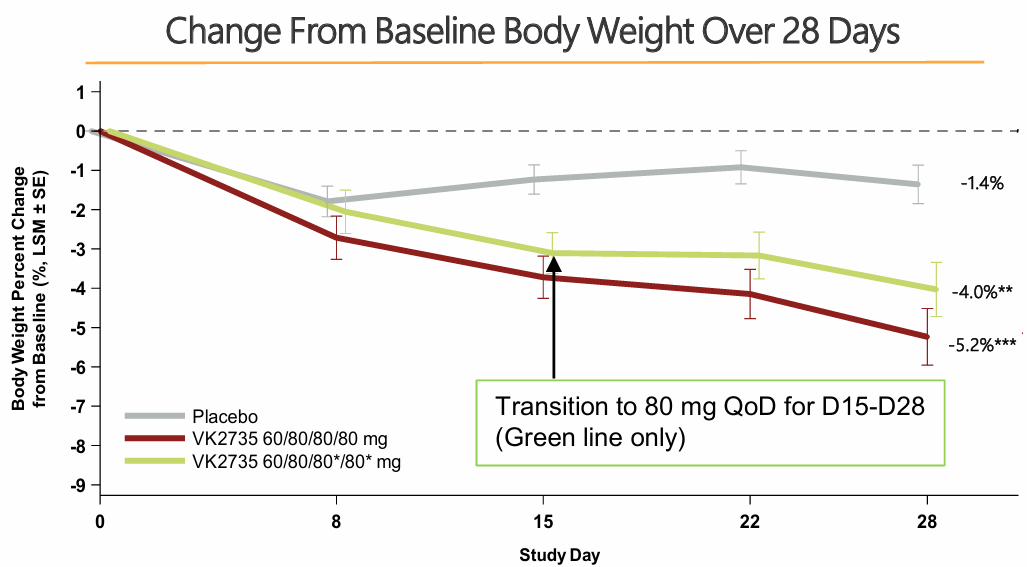
En cuanto a efectos secundarios, el único destacable son náuseas a dosis altas, que probablemente podría controlarse con incrementos paulatinos de la medicación.
Aunque los datos sean muy preliminares, podemos usarlos para conocer cómo se comporta el compuesto frente a la competencia. Ahora mismo, los principales competidores de VK2735 en su forma oral son la semaglutida de 25 mg y la Amicretina de Novo Nordisk. No incluyo Rybelsus porque se comercializa para la diabetes tipo 2, no para la obesidad. Eli Lilly también está desarrollando Orforglipron como pequeña molécula para tratar la diabetes, pero se trata de un agonista único de GLP-1R, no es un péptido y los últimos resultados que ha presentado no han sido muy prometedores.
Respecto a Novo Nordisk, esta ya comercializa Rybelsus para el tratamiento de la diabetes tipo 2, y ahora planea sacar al mercado una versión con más dosis de semaglutida oral para la pérdida de peso.
La comparación VK2735 vs. semaglutida resulta compleja dada la escasa información que ha compartido Novo Nordisk al respecto. Los ensayos de semaglutida oral (OASIS) son varios y la única publicación oficial es del ensayo OASIS 1, donde se usaron dosis de semaglutida de 50 mg, a diferencia de los 25 mg que han sido aprobados recientemente. Respecto a los ensayos con 25 mg, los únicos datos disponibles indican que los pacientes pierden un ~2% de peso a las 4 semanas, lo que quedaría por detrás de lo que puede conseguir Viking a partir de 20 mg.
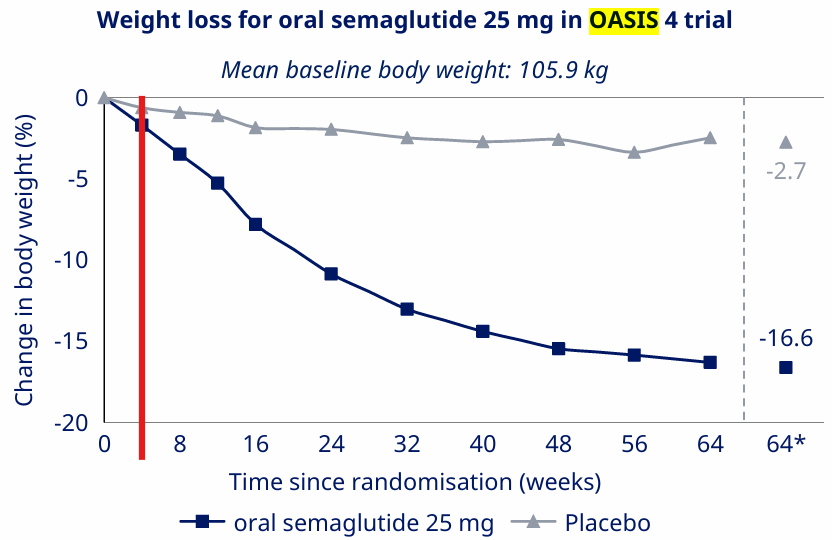
Si recurrimos a los datos del ensayo OASIS 1 de 50 mg de semaglutida, podemos establecer una “comparación” con los de VK2735 oral:
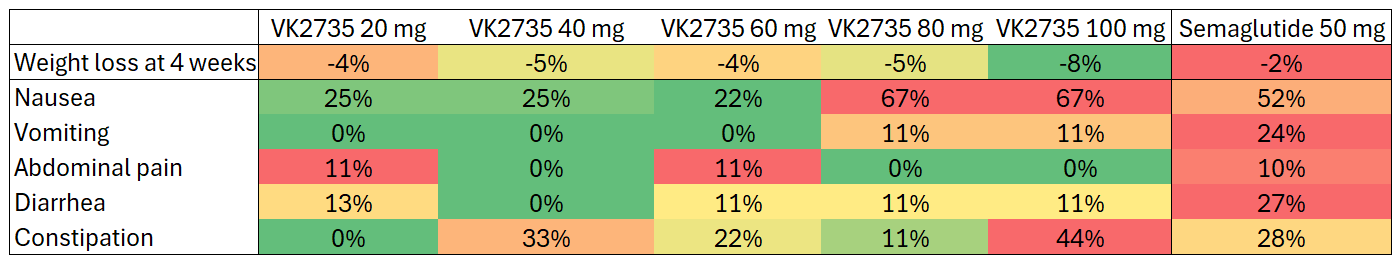
La comparación debe ser cuidadosa porque los efectos secundarios de la semaglutida se reportaron a las 68 semanas, mientras que el ensayo de VK2735 fue a las 4 semanas. El tiempo juega en contra de la aparición de efectos secundarios, por lo que es hasta curioso que en algunos efectos secundarios la semaglutida se comporte mejor que las dosis más altas de VK2735. No obstante, la diferencia en la pérdida de peso es sustancial a favor de VK2735. A esto también contribuye que el escalado de dosis de VK2735 es muy agresivo respecto a semaglutida:
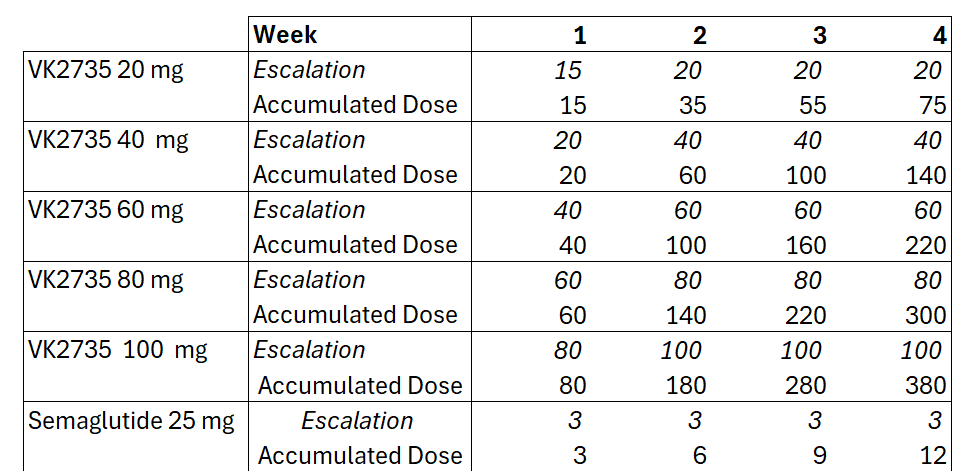
Esto provoca que la semaglutida se mantenga en su dosis más baja para cuando VK2735 ya ha sido administrado en grandes dosis. Aun así, la relativa tolerabilidad de VK2735 a pesar de las altas dosis es un buen indicio de que es más potente y mejor fármaco que la semaglutida. A este respecto deberían quedar pocas dudas, ya que la semaglutida sólo actúa frente a GLP-1R mientras que VK2735 añade además el agonismo hacia GIPR para potenciar la pérdida de peso. Lo mismo sucede con el fármaco oral de Eli Lilly para la pérdida de peso: Orforglipron. Este fármaco de tipo “pequeña molécula” estaba destinado a competir contra la versión oral de la semaglutida, pero decepcionó en ensayos clínicos al conseguir menor pérdida de peso que la propia semaglutida. Es de esperar que tampoco sea capaz de combatir a VK2735.
En cuanto a la comparación VK2735 / Amicretina, ambos compuestos se han probado en fase 1 para el tratamiento de la obesidad en su formato oral.
Los datos juegan muy a favor de Viking.
Si hacemos una comparación de los resultados de ambos fármacos, se observa que VK2735 consigue más pérdida de peso con menores efectos secundarios que la amicretina:
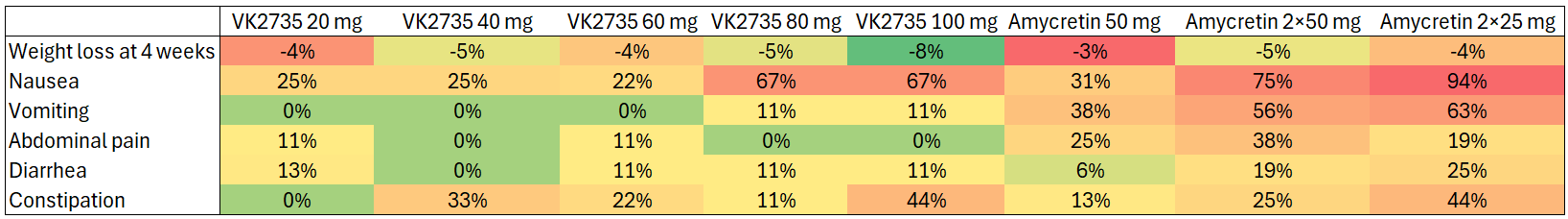
Aunque en esta comparativa es necesario hacer dos apuntes, uno a favor y otro en contra de Viking:
- El primero es que los datos de seguridad de la amicretina son del final del ensayo, una vez transcurridas 12 semanas, mientras que el de VK2735 duró 4 semanas. Esto juega a favor de Viking, ya que cuanto más largo el ensayo, más probabilidades de aparición de efectos secundarios.
- El segundo es que el escalado de dosis de VK2735 es mucho más agresivo que el de la amicretina, lo que haría aparecer más efectos secundarios si los hubiera:
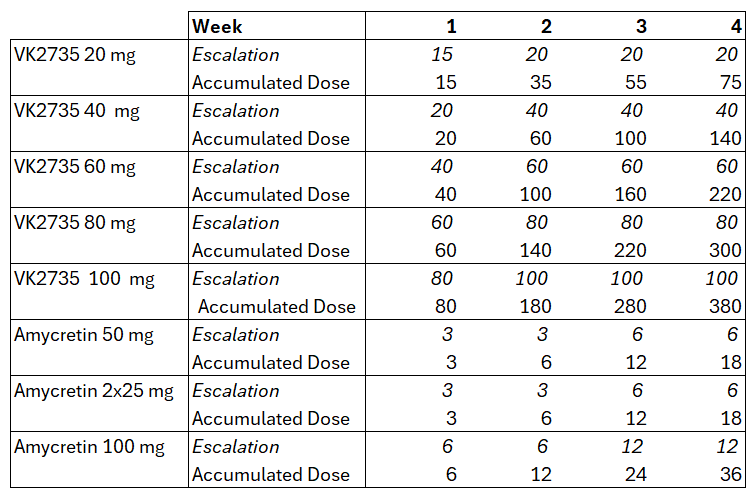
De modo que parece que, a pesar de ser un ensayo más corto que el de la amicretina, VK2735 lleva las de ganar en términos de eficacia/seguridad.
En cuanto a qué se deben estas diferencias, solo podemos especular por la diferencia de dianas farmacológicas. VK2735 actúa frente a GLP-1R y GIPR, mientras que la amicretina lo hace frente a GLP-1R y AMYR, lo que debe provocar más molestias gastrointestinales.
Estaría bien conocer qué estrategia emplea Viking para conseguir la absorción oral del compuesto. En el caso de Rybelsus, Novo Nordisk tuvo que recubrir la semaglutida con SNAC para conseguir que no se degradara en el estómago y que pudiera absorberse. El VK2735 parece absorberse solo, sin necesidad de otras moléculas que le ayuden, lo cual resulta llamativo.
Ensayo fase 2 (NCT06828055)
Este ensayo es el equivalente al anterior, pero para la versión oral:
| Diseño del estudio | |
|---|---|
| Fase | 2 |
| Pacientes | - Obesidad (BMI > 30) - Sobrepeso (BMI > 27) + afección relacionada |
| Ruta de administración | Subcutánea |
| Frecuencia | Diaria |
| Dosis | 15-120 mg |
| Duración | 13 semanas |
| Criterios de valoración | - Primario: pérdida de peso (%) - Secundario: proporción de sujetos que experimentan pérdidas de peso superiores al 5 y 10 % - Otros: Incidencia de efectos adversos |
Los resultados preeliminares aportados por Viking indican una pérdida de peso superior a la que ofrece cualquier fármaco en el mercado:
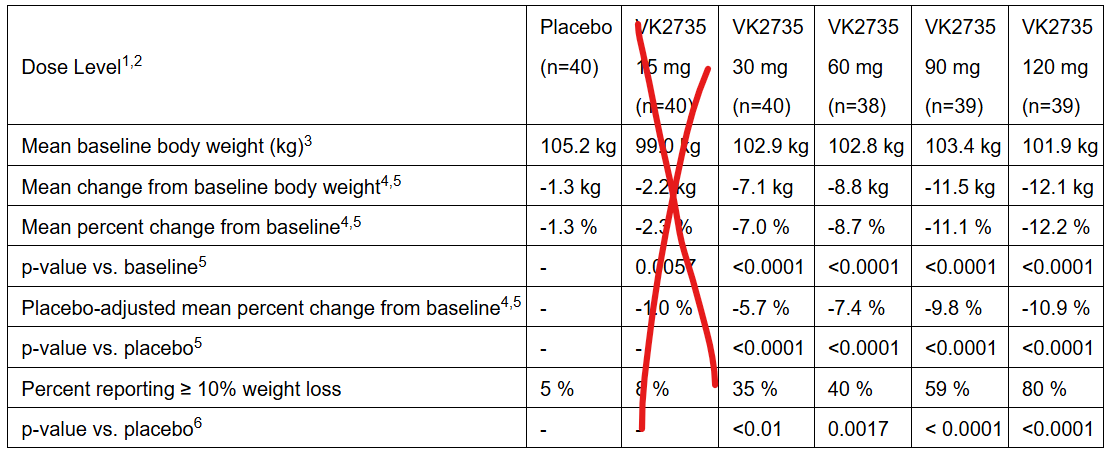
Sin embargo, los efectos secundarios han sido preocupantes y han provocado que a máximas dosis hasta un 20 % de los pacientes haya abandonado el tratamiento (ajustado por placebo):
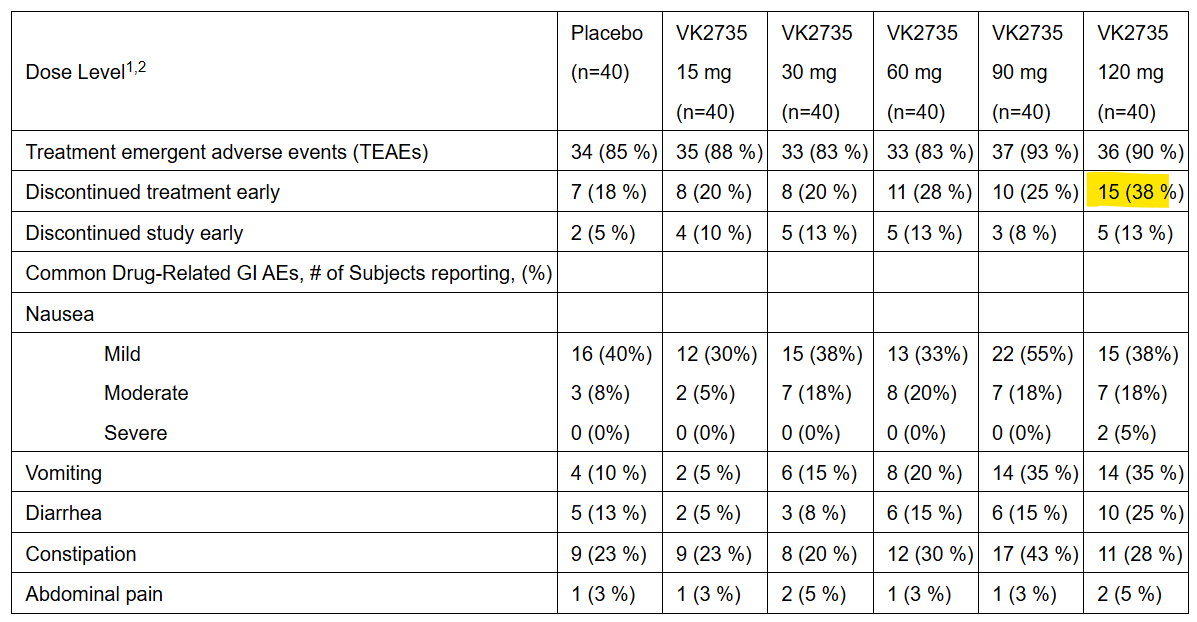
Varias reflexiones al respecto:
- Parece que el mayor problema que han tenido ha sido el escalado de las dosis del fármaco. Como veníamos comentando anteriormente, Viking sigue un escalado de dosis muy agresivo que en esta ocasión les ha afectado más de lo que pensaban. Un 20 % de abandonos es inaceptable y han comentado que para próximos ensayos controlarán más el escalado. Probablemente sacrifiquen algo de pérdida de peso por el camino, pero permitirá soportar mejor la terapia. Además, parece que los efectos adversos desaparecen en todos los grupos a partir de la 3 semana, lo que podría indicar el ajuste del cuerpo al tratamiento.
- No obstante, es llamativa también la cantidad de efectos secundarios que reportó el grupo placebo. El CEO de Vikings lo achaca a que muchos pacientes ya están al corriente de los efectos secundarios de estos fármacos y pueden verse más susceptibles a su posible aparición. Otro comentario del CEO de Vikings fue que en la dosis máxima los pacientes se estaban tomando 4 pastillas de 30 mg (120 mg en total), lo que seguramente no sería cómodo de administrar y no ayudaría a mantenerse en el ensayo.
- Si ajustamos los datos al placebo, veremos que VK2735 es muy competitivo en cuanto a pérdida de peso y prácticamente el mejor en su clase: Semaglutida y orforglipron no pueden competir al ser sólo análogos de GLP-1, mientras que la amicretina parece ser peor tolerada.
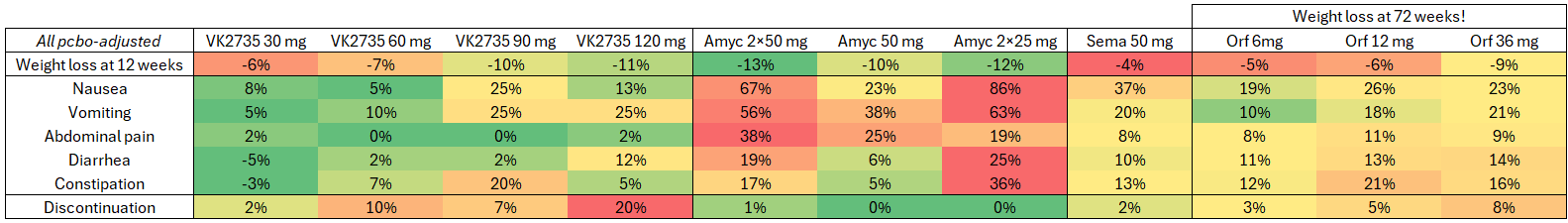
- Un subestudio de este ensayo probó además dosis de 90 mg seguidas de dosis bajas de 30 mg para mantenimiento, y comprobaron que la pérdida de peso se mantenía. Esto podría ser interesante desde el punto de vista del largo plazo: inducir una rápida pérdida de peso seguida de una dosis baja de mantenimiento con mínimos efectos secundarios.
Mi conclusión de este ensayo es que, si se usa un escalado de dosis más suave, las dosis de 30-90 mg de VK2735 podrían competir con la de amicretina de 50 mg por el puesto al mejor fármaco en desarrollo.
Ensayos fase 3
Los ensayos de fase 3 de VK2735 están destinados a evaluar la pérdida de peso en pacientes con obesidad y diabetes:
- VANQUISH-1 para pacientes con obesidad o sobrepeso.
- VANQUISH-2 para pacientes con diabetes y sobrepeso.
Los ensayos tendrán una duración de 78 semanas, por lo que tendremos que esperar a agosto de 2027 para conocer los resultados. Un punto importante es que estos ensayos van a realizarse exclusivamente en Estados Unidos. A diferencia de otros como los de la tirzepatida, que son globales, VK2735 sólo se probará en población estadounidense, lo que abaratará los costes pero también es posible que limite el mercado de este fármaco a Estados Unidos.
Además, está planeado comenzar un estudio a largo plazo en el que probar la versión subcutánea mensualmente y la versión oral semanalmente, con el objetivo de conocer si dosis más espaciadas servirían para que la gente mantuviera la adherencia al tratamiento. Recordemos que muchos pacientes tratados con análogos de GLP-1 abandonan el tratamiento al año, por lo que en ese filón hay mucho mercado por explotar.
VANQUISH-1 (NCT07104500)
| Diseño del estudio | |
|---|---|
| Fase | 3 |
| Pacientes | - Obesidad (BMI > 30) - Sobrepeso (BMI > 27) + afección relacionada - NO diabéticos |
| Ruta de administración | Subcutánea |
| Frecuencia | Semanal |
| Dosis | 7,5 / 12,5 / 17,5 mg |
| Duración | 78 semanas |
| Criterios de valoración | - Primario: pérdida de peso (%) - Secundario: proporción de sujetos que experimentan pérdidas de peso superiores al 5 y 10 % |
VANQUISH-2 (NCT07104383)
| Diseño del estudio | |
|---|---|
| Fase | 3 |
| Pacientes | - Obesidad (BMI > 30) - Sobrepeso (BMI > 27) + afección relacionada - NO diabéticos |
| Ruta de administración | Subcutánea |
| Frecuencia | Semanal |
| Dosis | 7,5 / 12,5 / 17,5 mg |
| Duración | 78 semanas |
| Criterios de valoración | - Primario: pérdida de peso (%) - Secundario: proporción de sujetos que experimentan pérdidas de peso superiores al 5 y 10 % |
En cualquier caso, si los datos de la fase 3 confirman lo visto en la fase 2, VK2735 podría competir con la tirzepatida por el mercado de análogos duales GLP-1/GIP.
Probabilidades de éxito
Recordemos que en este apartado no evalúo las probabilidades de éxito del compuesto en cuanto a ganancia de cuota de mercado, sino si la ciencia avala que el medicamento funcione.
Como VK2735 se está formulando de dos maneras distintas, es justo analizarlas por separado. Comencemos por la versión subcutánea.
Versión inyectable
Premisas:
- Los receptores de GLP-1 y GIP son relevantes para tratar la obesidad y el sobrepeso.
- VK2735 se une a los receptores de GLP-1 y GIP con alta afinidad para inducir pérdida de peso.
- VK2735 consigue una pérdida de peso igual superior a la tirzepatida.
- VK2735 produce menos efectos secundarios que la tirzepatida.
Premisa 1: 100 %
Ya hemos analizado en Sinapsis la importancia de estos dos receptores en el control de la obesidad:
Ambas dianas farmacológicas están ampliamente validadas en la literatura científica y en ensayos clínicos. La aprobación de la tirzepatida es la prueba indiscutible de ello.
Premisa 2: 100 %
La mejor evidencia preclínica de que el VK2735 se une a los receptores de GLP-1 y GIP proviene de la propia compañía. A esto hay que sumarle los datos clínicos que parecen avalar los datos preclínicos. Si bien no existe apenas información sobre el mecanismo de acción del fármaco ni estudios realizados por laboratorios independientes, parece complicado que los pacientes pudieran perder tanto peso en los ensayos clínicos si el mecanismo molecular no fuera el que se espera del compuesto.
Premisa 3: 75 %
Esta y la siguiente son quizás las premisas más importantes. Si el VK2735 aspira a ganar presencia en el espacio de la obesidad, debe presentar una alternativa superior al fármaco estrecha que está inundando el mercado: la tirzepatida. Si consigue lo mismo, no supondrá ningún avance respecto a lo que ya existe y ya se comercializa.
Si consigue una pérdida de peso similar a la de la tirzepatida, su potencial de mercado se verá severamente comprometido. Pero si consigue superarlo, se convertirá en la mejor molécula en su clase. Y por eso sí que se paga un buen premium.
Mientras que la tirzepatida provoca una pérdida de peso del ~8% a las 13 semanas, el VK2735 sube este porcentaje hasta el 14,7 %. La diferencia es radical, lo cual es cuanto menos curioso dado que ambas moléculas se unen a los mismos receptores. La estructura de VK2735 debe estar sumamente optimizada para conseguir esta diferencia tan grande (un usuario en Twitter sugirió que VK2735 es idéntico a la tirzepatida y que la única diferencia reside en el ácido graso que se emplea para conseguir su unión a la albúmina). Pero no podemos cegarnos por este simple dato. Tengamos en cuenta que estamos comparando ensayos distintos y de distintas fases (fase 2 vs 3). No es correcto hacer comparaciones directas, pues no son pocas las moléculas que muestran ser eficaces en la fase 2 pero decepcionan en la fase 3.
La probabilidad de que la premisa 3 se cumpla es, a lo sumo, del 75 %. Debemos ser cautelosos hasta que nueva evidencia justifique mayor confianza en el fármaco.
Premisa 4: 75 %
Por último, otro frente en el que VK2735 podría ser competitivo no es en conseguir más eficacia que la tirzepatida, sino en tener un perfil de seguridad mayor. Actualmente, los fármacos basados en análogos de GLP-1 ocasionan muchas molestias en el tracto gastrointestinal. Molestias severas y manejables, pero al fin y al cabo molestias que limitan su adopción por una mayoría de la población afectada.
En este sentido, los datos de seguridad de VK2735 parecen ser similares a los de la tirzepatida o ligeramente superiores, lo que podría suponer un impulso adicional secundario para su aprobación. En este punto, volvemos a incidir igual que en la premisa 3: necesitamos datos de fase 3 que avalen lo visto en la fase 2, con una población mayor y más diversa. Por el momento, otorgar un 75 % de éxito a esta premisa parece conservador.
Probabilidades de éxito de VK2735 subcutáneo:
Vamos con la versión oral.
Versión oral
Las premisas son las mismas que para la versión subcutánea, pero con una adicional:
- VK2735 mantiene la eficacia al ser administrado de forma oral.
Premisa 5: 50 %
Me explico.
Las versiones inyectables de estos fármacos han demostrado ser eficaces de manera consistente. No hay duda de que funcionan. Por eso, no merece la pena valorarlo al hablar de la versión subcutánea.
No obstante, las versiones orales de péptidos son sumamente difíciles de administrar. Al hablar de Rybelsus ya explicamos los motivos por los que administrar péptidos orales requiere salvar muchos obstáculos.
Novo Nordisk emplea SNAC para facilitar la entrada del péptido en el organismo, y la efectividad es inferior a la de la vía subcutánea. Viking no ha especificado de qué manera han conseguido que el VK2735 pueda ser absorbido de manera oral, y los únicos datos de los que disponemos actualmente son de un ensayo de fase 1. Es cierto que este ensayo ha aportado buenos datos y parece que el compuesto se absorbe y cumple su función, pero sigue siendo un ensayo de fase 1 y partimos con más incertidumbre que con la versión subcutánea. Si los datos se confirman en posteriores estudios, el VK2735 sería el primer agonista dual en ser aprobado para la administración oral. Mientras tanto, la versión de semaglutida oral de 25 mg ya ha demostrado conseguir un 16 % de pérdida de peso en ensayos clínicos 6.
Por tanto, las probabilidades de que la absorción permita que el fármaco sea eficaz son, por el momento, del 50 %.
Probabilidades de éxito de VK2735 oral:
Competidores
La competición en el mercado de la diabetes y la obesidad es inmensa. No en vano, es un mercado que aspira a valer cientos de miles de millones en menos de 10 años.
Novo Nordisk fue la pionera en el segmento de los análogos de GLP-1, pero la competencia no se ha quedado atrás. He elaborado una tabla con los competidores actuales a los que se enfrenta VK2735:
| Drug Name | Development Stage | Efficacy (% Weight Loss) | Primary Safety Concerns |
|---|---|---|---|
| Amycretin | Phase 2-3 | 22.0% at 37 weeks | GI adverse events |
| CagriSema (cagrilintide/semaglutide) | Phase 3 | 22.7 at 68 weeks | GI: nausea |
| Efocipegtrutide | Phase 2 | N/A | GI disturbances |
| Retatrutide | Phase 3 | 24.2% at 48 weeks | GI & Cardiac side effects |
| Semaglutide | Approved | 20.7% at 72 weeks | GI: nausea, diarrhea |
| Tirzepatide | Approved | 20.9% at 72 weeks | GI: nausea, diarrhea |
| UBT251 | Preclinical | N/A | GI adverse events |
| VK-2735 | Phase 3 | 14.7% at 13 weeks | GI, minimal |
| VK-2735 | Phase 2 | 8.2% at 4 weeks | GI, minimal |
¿Qué diferencia a VK2735 de la competencia? En las versiones subcutáneas, poco respecto a la tirzepatida.
Los datos del ensayo de fase 2 nos indican que VK2735 podría ser algo más potente que tirzepatida y eso le permitiría conseguir una modesta reducción de peso superior o ahorrarse dinero en la producción del fármaco. Respecto a los demás análogos de GLP-1, la ventaja de VK2735 es que tener como diana a GLP-1/GIP es más potente que GLP-1/AMYR o GLP-1 a solas le podría hacer ganar cuota de mercado frente a estos.
Lo interesante puede que se encuentre en la versión oral del compuesto, ya que la competencia es menos feroz y ningúna otra empresa está desarrollando un análogo dual GLP-1/GIP en formato oral que esté avanzado y presente tan buen perfil de seguridad/eficacia.
Potencial de mercado
Procedemos ahora a asumir el potencial de mercado de VK2735. Antes de empezar, dos avisos:
Aviso
- Todo lo aquí contenido tiene un carácter informativo y nunca debe ser interpretado como consejo de inversión.
- Los modelos al final son solo eso: modelos. Y como tales, todos los modelos son erróneos. Lo importante es que algunos pueden errar menos que otros y sernos útiles.
Para hallar el valor, empleo la fórmula:
Pacientes potenciales
Empecemos definiendo la población susceptible de ser tratada:
- Se estima que para 2030 habrá 100 millones de estadounidenses con obesidad (BMI > 30). No podemos tener en cuenta otros países porque los ensayos de fase 3 se están llevando a cabo exclusivamente en Estados Unidos, lo que limita potencialmente la aprobación por otras agencias reguladoras.
- Dada la facilidad con la que una persona puede ser diagnosticada de la obesidad, suponemos que un gran porcentaje de la población será diagnosticada: 70 millones diagnosticados.
- El porcentaje de población estadounidense obesa que recibe análogos de GLP-1 no alcanza el 3% actualmente, pero esta cifra debería crecer a medida que se acumule más evidencia de su eficacia y seguridad. El requisito para poder tratarse con estos análogos sería tener un BMI > 30 (o > 27 + alguna otra enfermedad), por lo que el potencial es enorme. Asumamos que, a largo plazo, unos 40 millones de pacientes cumplirían los criterios médicos para recibir esta terapia.
- Pensemos que algunos de estos pacientes no podrán recibir el tratamiento, ya sea porque su seguro no lo cubre, porque no está disponible donde vive, o porque no puede costearlo. Siendo conservadores, podríamos asumir que un 25 % de los pacientes podrían recibir el tratamiento.
- Por último, debemos decidir si VK2735 podrá ser aprobado también para tratar la diabetes, lo que podría duplicar los pacientes potenciales. Los ensayos de fase 3 actuales están dirigidos a reducir el peso en personas con obesidad o diabetes de tipo 2, pero entre los criterios de valoración no se incluyen biomarcadores que midan mejoría en la diabetes como, por ejemplo, el porcentaje de hemoglobina glicosilada. Mientras no se modifiquen los criterios o se anuncien nuevos ensayos específicos para la diabetes, opto por no incluir este mercado en la valoración.
Esto nos deja una cifra de 10 millones de pacientes susceptibles de recibir el fármaco.
Cuota de mercado
Ahora, también debemos incorporar cuál creemos que será el porcentaje de pacientes susceptibles que terminará recibiendo una prescripción de VK2735. Aquí debemos tener en cuenta el tipo de mercado en el que nos encontramos: altamente competitivo.
Ya existen varias opciones viables en el mercado y otras tantas están en desarrollo. Multitud de médicos están familiarizados con la semaglutida y la tirzepatida, pero desconocen el VK2735. La eficacia y seguridad del compuesto debe ser muy fuerte para que un médico comience a recetarlo a nuevos pacientes o incluso cambie a sus pacientes ya tratados a este nuevo fármaco. Por tanto, lo esperable sería que VK2735 pudiera capturar un 5-10% de la demanda del mercado.
Si pensamos en la versión oral, esta siempre tendrá una mejor aceptación por parte del mercado, ya que todo el mundo prefiere tomarse una pastilla a inyectarse un medicamento. Además, los datos clínicos hasta la fecha prometen situarlo como el mejor de su clase, lo que podría estimular una mayor demanda del producto. Sería viable asignarle un 10-15 % de la demanda del mercado, un poco por encima de la versión subcutánea.
Precio anual
Afortunadamente, podemos comparar los precios de los fármacos ya disponibles en el mercado para hacernos a la idea de cuánto podría costar esta terapia. El precio bruto de Wegovy y Mounjaro ronda los 1.000 /mes usando descuentos, seguros, y otras formas de reducir el precio. Dada la novedad de VK2735, y si su eficacia acompaña, el producto podría ofrecerse por precios ligeramente superiores de entre 750-1000 .
Las versiones orales “suelen” ser algo más baratas por la diferencia en el método de administración (al fin y al cabo, los autoinyectores también cuestan), de modo que podríamos esperar que la versión oral de VK2735 se comercializara por un precio ligeramente inferior.
Juntándolo todo y ajustando por la probabilidad de éxito de cada versión, obtengo las siguientes estimaciones como pico de ventas anual:
- “Bear-scenario”: asume que el fármaco será inferior a tirzepatida y poca gente lo preferirá.
- “Base-case scenario” implica que VK2735 sea capaz de diferenciarse de la tirzepatida en su forma subcutánea y que la forma oral mantenga lo observado en los ensayos de fase 1.
- Finalmente, el “bull-scenario” sería aquel en el que VK2735 se diferencie mucho de tirzepatida en términos de seguridad y/o eficacia y pueda capturar mayor cuota de mercado.
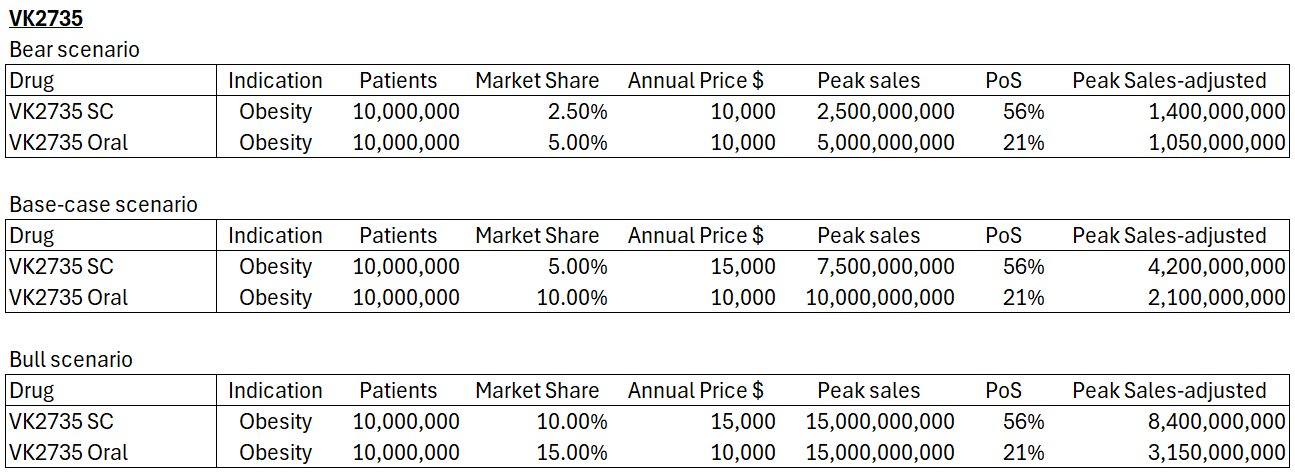
En comparación con fármacos como Wegovy o Mounjaro que esperan un pico de ventas de 25.000 M$, las estimaciones de VK2735 parecen conservadoras. Pero recordemos factores como la limitación geográfica, el cuello de botella que pueda suponer la manufactura del fármaco, y que VK2735 sería un rival directo de la tirzepatida. A la espera de que tengamos nuevos datos que aumenten las probabilidades de éxito del fármaco, prefiero optar por la prudencia.
Conclusión
VK2735 constituye un prometedor agonista dual de los receptores de GLP-1/GIP. La evidencia clínica hasta la fecha sugiere una eficacia comparable o superior a lo existente actualmente en el mercado en términos de pérdida de peso. No obstante, es el perfil de seguridad lo que le podría hacerle destacar frente a la competencia.
Sin embargo, el fármaco no está exento de riesgos de ejecución para conseguir su aprobación. Ya hemos visto como un pequeño fallo puede condenar todo un ensayo al fracaso, por lo que en los próximos años deberemos estar atentos a la ejecución de Viking Therapeutics en los ensayos clínicos y en el entorno regulatorio.