Cuando pensamos en desarrollar terapias para enfermedades, hay un elemento que debería ser el centro de atención:
El paciente.
Puedes tener un fármaco milagroso.
Pero si el paciente no se lo toma, será un fármaco milagroso inútil.
Hay muchas causas que podrían llevar a que un paciente no siga la pauta de administración de un medicamento. Puede que los efectos secundarios sean más incómodos de tolerar que la propia enfermedad o que la administración del fármaco sea tediosa (no poder ser ingerido con alimentos, tener que acudir a un hospital para su administración, etc).
En cualquier caso, la consecuencia será que el paciente no tomará la medicación y habrá un problema de falta de adherencia al tratamiento.
La adherencia al tratamiento
La adherencia a la terapia hace referencia a cómo un paciente sigue un régimen médico propuesto. Es decir, nos dice si un paciente está siguiendo las indicaciones médicas para tratar su enfermedad.
La adherencia es clave para conseguir que los pacientes sigan las pautas marcadas al pie de la letra y tratar lo mejor posible su enfermedad. Sin embargo, algunas terapias pueden ser tediosas de cumplir. Este concepto es tenido muy en cuenta por la industria farmacéutica a la hora de desarrollar fármacos.
¿Cómo mejoramos la adherencia al tratamiento?
Formas hay muchas, pero una que funciona muy bien es producir medicamentos que se tomen por vía oral.
Por eso, en el artículo de hoy hablaremos de:
- Los problemas de la administración de péptidos orales.
- La estrategia que siguió Novo Nordisk para superar esos problemas.
Al lío.
Los problemas de la vía oral
La ruta oral suele ser la preferida por los pacientes.
Evita tener que pincharse, echarse ungüentos que dejan la piel pringosa y pueden dar reacción, o tener que ir al hospital a inyectarse el medicamento en vena. Lo único que hay que hacer es tomarse una pastilla cada cierto tiempo.
Rápido, cómodo y sencillo de entender.
Entonces, ¿por qué los análogos de GLP-1 como la semaglutida se administran de forma subcutánea (por debajo de la piel)?
Porque lo que no es sencillo es sortear la hostilidad del tracto gastrointestinal.

Pongámonos en situación: eres una molécula de semaglutida. Tu destino final es ser ingerida y llegar intacta al sistema digestivo para ser absorbida y poder alcanzar el torrente sanguíneo, desde donde te distribuirás al resto del organismo.
Problemas:
En primer lugar, la estructura de muchos de estos péptidos activa el sabor amargo en las papilas gustativas de la boca, lo que produce respuestas de aversión en el paciente a la hora de tomarlos.
En segundo lugar, los cambios bruscos de pH que ocurren en el sistema digestivo afectan a la estabilidad de los péptidos. La insulina, por ejemplo, forma agregados insolubles en el pH ácido del estómago, mientras que el pH básico del duodeno produce la precipitación de hormonas como la calcitonina. Si se vuelven insolubles, estas moléculas no pueden ser absorbidas.
En tercer lugar, nuestro sistema digestivo está plagado de proteasas. La función de las proteasas es la de digerir los alimentos para absorber los nutrientes, pero no diferencian entre sustratos: no saben si los enlaces que están rompiendo provienen de las fibras musculares de un filete o de un medicamento. Como consecuencia, los péptidos son presa fácil de estas proteínas y no llegan a ser absorbidos en el intestino.
Por último, el intestino posee una capa mucosa en su interior. Esta mucosa ayuda a proteger a las células del intestino de la acción de las enzimas del páncreas, pero también limita la difusión de los péptidos a través de ella. Además, el tamaño de los péptidos dificulta su absorción. Los péptidos son moléculas relativamente grandes, por lo que no pueden pasar a través de los huecos entre las células para llegar a la sangre. Su única opción es ser absorbidos por las células del intestino y después liberados al torrente sanguíneo, pero esta ruta tiene limitaciones y también produce su degradación.
En conjunto, todos estos problemas provocan que la cantidad de péptido absorbido sea ridículamente insignificante. A esto, tenemos que sumarle que la estabilidad de estos péptidos en la sangre es muy reducida (hablé aquí sobre ello).
Entonces, ¿cómo consiguió Novo Nordisk la aprobación de su versión oral de semaglutida?
La ciencia tras el éxito de Rybelsus®
Rybelsus® fue el primer péptido oral para el tratamiento de la diabetes tipo 2 aprobado por la FDA y la EMA en 2019 y 2020, respectivamente.
El razonamiento tras Rybelsus es sencillo: si ya tenemos un péptido (semaglutida) con unos efectos asombrosos para el control de la glucosa y el peso, ¿cómo podríamos mejorar la adherencia de los pacientes?
Generando una formulación oral que evite que los pacientes tengan que pincharse.
Dado que la semaglutida ya de por sí es efectiva, solamente era necesario solventar dos problemas:
- Mejorar la absorción de la semaglutida en el tracto gastrointestinal.
- Proteger a la semaglutida de la degradación hasta su absorción.
La solución se encontró en el salcaprozato de sodio (SNAC).
Veámoslo en mayor profundidad.
Un potenciador de la permeabilidad y protector de la semaglutida
Las células del tracto gastrointestinal están fuertemente unidas entre sí para evitar el paso no selectivo de moléculas hacia el torrente sanguíneo. Así, el contenido ácido del estómago o los alimentos del intestino no pueden filtrarse hacia el interior del organismo.
Aunque este fenómeno nos protege, también dificulta la absorción de la semaglutida. Por ello, el SNAC (N-[8-(2-hydroxybenzoyl)amino] caprylate) actúa como un potenciador de la permeabilidad.
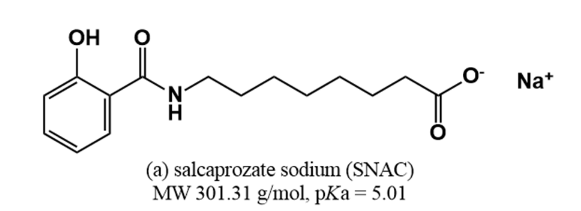
De manera resumida, compuestos como la semaglutida son bastante hidrofílicos, por lo que no pueden atravesar bien las membranas celulares (que son lipofílicas, ricas en grasas). El principio es el mismo por el que el agua y el aceite no se juntan cuando los mezclas. Aquí es donde entra en juego el SNAC, cuya función es unirse a estos compuestos y mejorar su lipofilicidad. De esta manera, el SNAC favorece que estos compuestos atraviesen las membranas celulares y puedan pasar al torrente sanguíneo.
En el caso de la semaglutida, la función del SNAC es ligeramente distinta, aunque la consecuencia final es la misma: mejorar la absorción de la semaglutida y su disponibilidad en la sangre.
El siguiente artículo lo demuestra de manera muy clara y visual:

En este estudio, elaborado por científicos de Novo Nordisk, trataron de caracterizar la eficacia de SNAC para administrar semaglutida de forma oral.
En primer lugar, observaron que la coadministración de semaglutida con SNAC en forma de pastilla conseguía:
- Disolverse en el estómago (apartado A). Se puede apreciar como la pastilla, al principio concentrada en la parte inferior del estómago, se va expandiendo y difundiendo por toda la cavidad.
- Elevar los niveles de semaglutida en sangre durante horas (apartado B). Esta gráfica compara la concentración de semaglutida en sangre en función del tiempo transcurrido. Se ve cómo poco después de la administración se produce un pico de semaglutida que va disminuyendo paulatinamente.
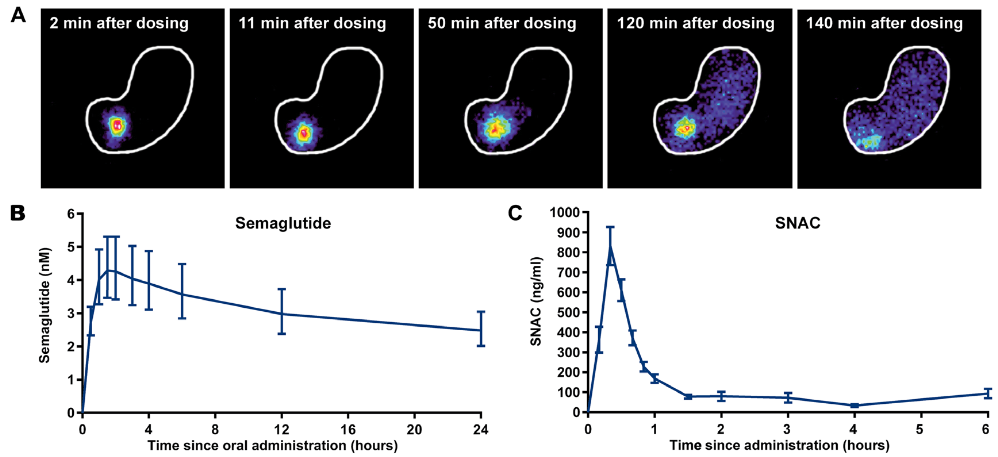
Este experimento nos indicaba por un lado, que la semaglutida sobrevivía sin degradarse en el estómago, y que la mayor parte de la absorción de la semaglutida ocurría en este órgano y no en el intestino. Y esto es más importante de lo que pueda parecer: la absorción en el estómago nos evita “el efecto de primer paso”, un fenómeno por el cual algunos medicamentos administrados por vía oral apenas consiguen llegar al torrente sanguíneo. Las causas son muchas, pero principalmente que los medicamentos que se absorben en el intestino pasan primero por el hígado antes de liberarse al resto del cuerpo. El hígado está especializado en filtrar y degradar sustancias potencialmente tóxicas (como muchos fármacos), y esto inutiliza muchos medicamentos. Al conseguir una absorción en el estómago, se evita el efecto de primer paso y se puede lograr una mayor concentración de semaglutida en sangre.
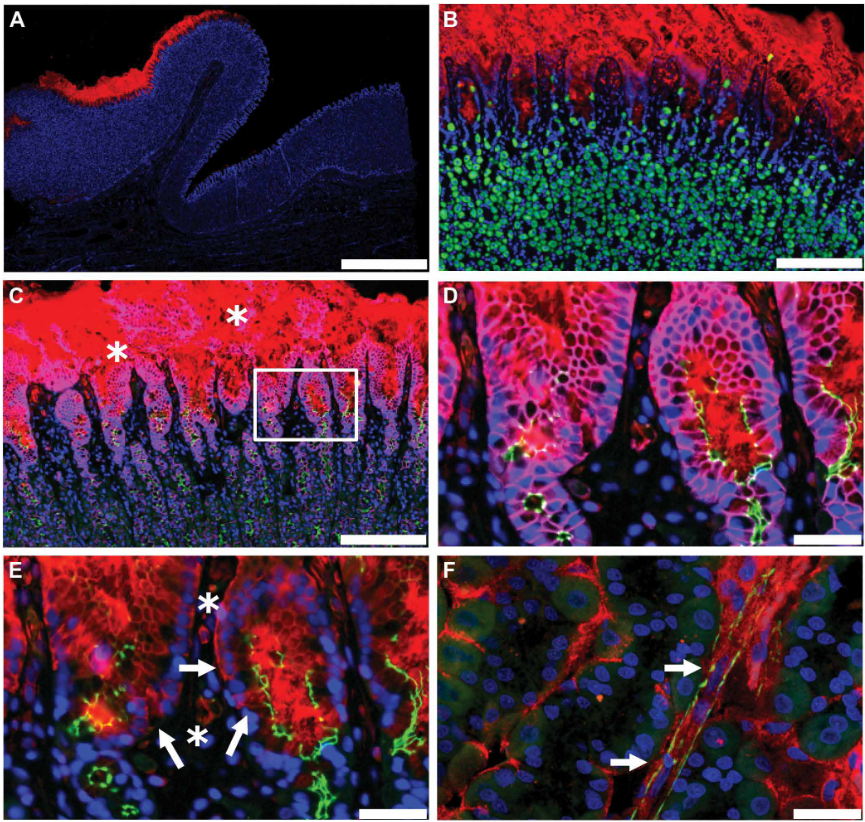
Un vistazo en mayor profundidad permitió comprobar el proceso de absorción de la semaglutida en el estómago. En la siguiente imagen, se puede apreciar el estómago de un perro al que se le ha administrado una pastilla de semaglutida con SNAC:
- El apartado A muestra la estructura a grandes aumentos del estómago. No tienes que conocer los detalles, basta con saber que está formado por muchas capas de células apiladas unas encima de otras. La parte superior correspondería al interior del estómago, donde se observa en color rojo la semaglutida, y en azul los núcleos de las células. El color verde tampoco viene a cuento, permite identificar algunos tipos específicos de células.
- En el apartado D, un vistazo a mayores aumentos permite observar que la semaglutida se encuentra dentro de las células. Es decir, que ha sido absorbida por las células del estómago.
- Y finalmente, en el apartado F podemos ver la estructura alargada de un vaso sanguíneo lleno de semaglutida (flechas blancas). Es decir, la semaglutida no solo sobrevive y penetra en el estómago, sino que además se traspasa al torrente sanguíneo.
Aunque aun quedaba una pregunta por resolver: ¿cómo podía el SNAC proteger a la semaglutida de la degradación en el estómago?
Ya hemos visto que el estómago es un infierno para los péptidos: un pH muy ácido y la presencia de proteasas como la pepsina. Sin embargo, el SNAC actuaba de una manera curiosa: tras ser ingerida la pastilla, el SNAC se disolvía y generaba un incremento del pH de forma local.
En cristiano, este incremento del pH generaba una atmósfera protectora localizada que inactivaba la pepsina y permitía que la semaglutida pudiera ser absorbida sin ser degradada.
En conjunto, la función del SNAC era dual:
- Protegía a la semaglutida de la degradación.
- Favorecía su absorción en el estómago.
De esta manera, Novo Nordisk había conseguido una versión oral y efectiva de la semaglutida para el tratamiento de la diabetes tipo 2.
Un jarro de agua fría
A pesar de lo impresionante del compuesto y lo maravillosas que pueden ser algunas mentes científicas, Rybelsus® no es perfecto.
Una administración más compleja
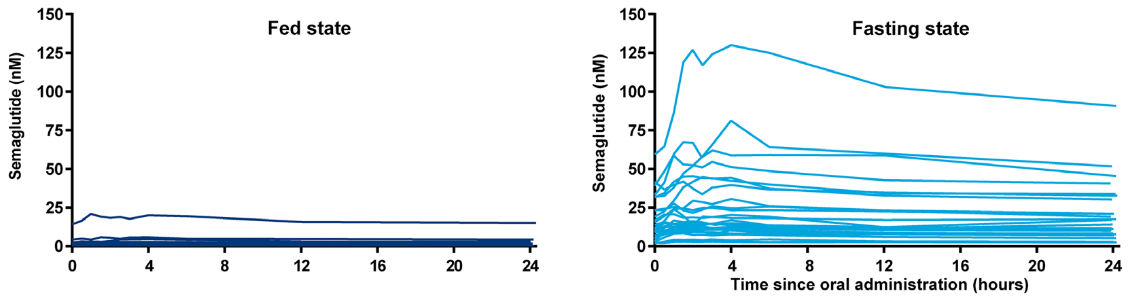
En el mismo artículo se estudia si la ingesta de la pastilla con comida puede afectar su absorción en el estómago. Tristemente, así sucede. La administración de Rybelsus junto con comida produce que su absorción sea nula.
La siguiente gráfica muestra la poca cantidad de semaglutida que alcanza la sangre cuando la pastilla se administra con comida (fed state) vs cuando se ingiere con el estómago vacío (fasting state):
Por este mismo motivo, en el prospecto de Rybelsus figura que el fármaco debe ser tomado con el estómago vacío, no haber comido 8 horas antes y esperar al menos media hora para ingerir alimentos.
En cambio, las versiones inyectables son más “cómodas” de usar. Un pinchazo a la semana y listo.
La dosis
La versión comercializada de Rybelsus contiene entre los 3 y 7 mg de semaglutida y puede llegar hasta 50 mg AL DÍA.
Por comparación, la dosis de semaglutida en la versión inyectable (Ozempic) varía entre 0,25 y 4 mg A LA SEMANA.
Las concentraciones de semaglutida necesarias para conseguir una dosis efectiva en sangre son mucho más elevadas cuando este se administra de forma oral en vez de inyectada. Por mucho que la absorción haya mejorado, algunos estudios estiman que la cantidad de semaglutida que alcanza el torrente sanguíneo es de apenas el 1% de toda la cantidad contenida en la pastilla. El exceso de fármaco que no se absorbe o no alcanza la sangre también puede suponer mayores efectos secundarios, ya que existen receptores de GLP-1 distribuidos por todo el tracto gastrointestinal.
Además, los inyectables tienen una ventaja: la inyección subcutánea permite que la piel actúe como un reservorio de semaglutida que se va liberando paulatinamente a lo largo de la semana. Con la versión oral, lo que atraviesa el estómago entra directamente al torrente sanguíneo y se consume; de ahí que tenga que ser tomado de forma diaria.
Para Novo Nordisk, la formulación oral implica una enorme expansión de la capacidad productiva con la que ser capaces de generar semaglutida en cantidades ingentes.
Ambos factores suponen barreras a la adopción de Rybelsus, ya sea por escasez de oferta o falta de demanda. Sin embargo, la realidad es que el fármaco se ha comercializado con éxito, por lo que sus efectos positivos deben ser superiores a los negativos. Pero, ¿es mejor que Ozempic?
Rybelsus vs Ozempic
La realidad es que las ventas de Ozempic superan con creces a las de Rybelsus:
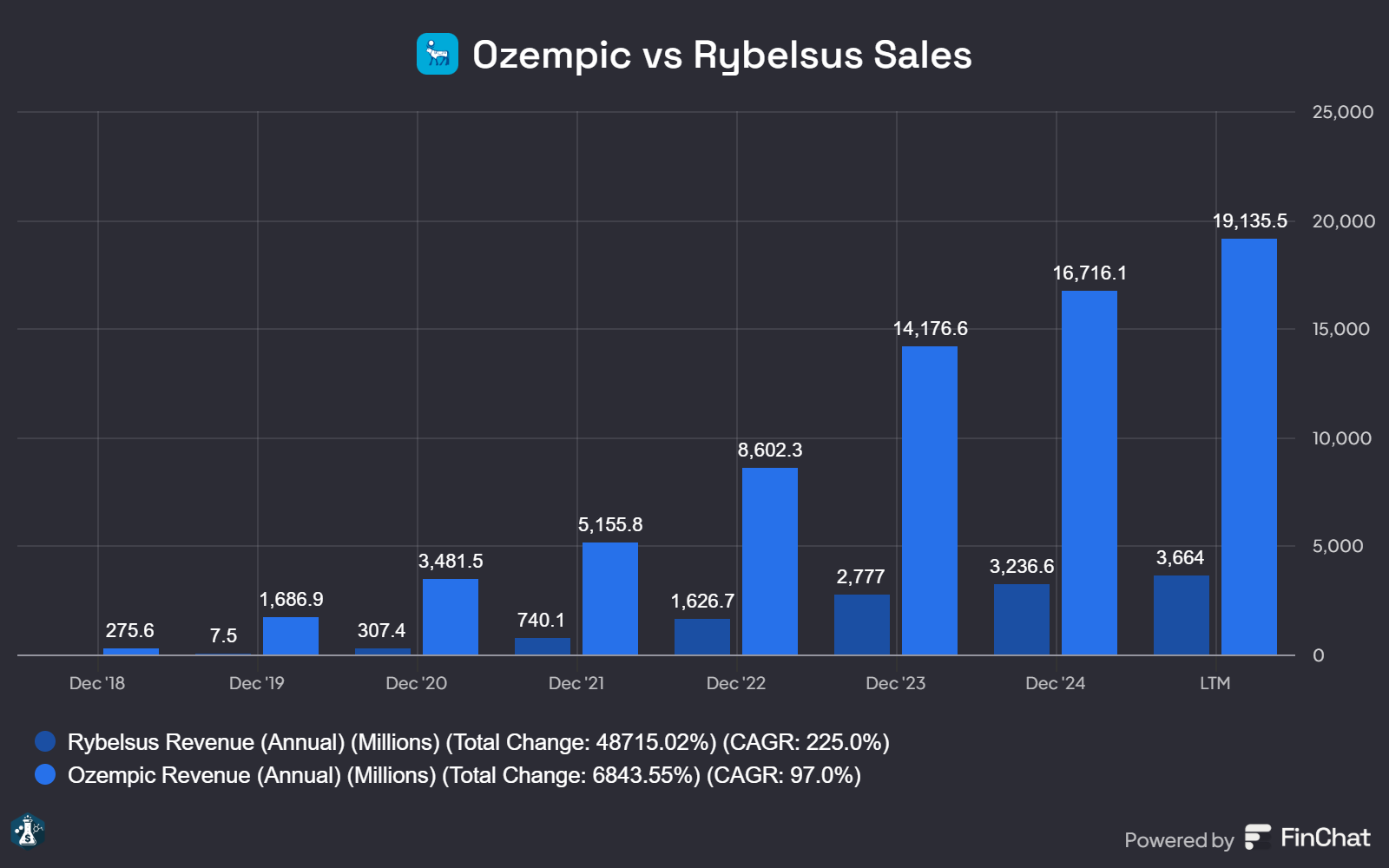 He decidido comparar Ozempic vs Rybelsus porque ambas están indicadas para el tratamiento de la diabetes tipo 2. La diferencia de dosis de Wegovy complicaría la comparación de forma innecesaria dado que está indicado exclusivamente para el sobrepeso.
He decidido comparar Ozempic vs Rybelsus porque ambas están indicadas para el tratamiento de la diabetes tipo 2. La diferencia de dosis de Wegovy complicaría la comparación de forma innecesaria dado que está indicado exclusivamente para el sobrepeso.
Las causas tras esta diferencia de ventas pueden ser variadas:
- En torno al 70 % de los pacientes suele preferir las medicaciones orales sobre las inyecciones por motivos de comodidad. Sin embargo, un estudio observó que tras informar a los pacientes sobre la pauta de administración de Rybelsus, el porcentaje disminuyó hasta el 50 % frente a la versión inyectable.
- Aunque ambos tienen los mismos efectos secundarios, puede que Rybelsus tenga una mayor incidencia de estos (pero no he encontrado evidencia que lo confirme).
- Puede que la mayor cantidad de semaglutida requerida en la formulación de Rybelsus haya frenado su expansión frente a Ozempic.
- Y también puede que la aprobación más temprana de Ozempic haya generado una mayor adopción de esta forma de tratamiento frente a la de Rybelsus.
En el futuro, se estima que la adopción de Rybelsus sea mayor y crezca a mayor ritmo que la de Ozempic (8 % para Ozempic vs >15 % para Rybelsus), aunque me cuesta creer que pueda superar el mercado total de esta.
Con esto no quiero decir que ambos fármacos compitan entre sí. Mi opinión es que Novo Nordisk ha sabido entender las necesidades de algunos pacientes y ha decidido introducir la versión oral para expandir su mercado a aquellos pacientes que por diversas razones no podían o querían usar las versiones inyectables de semaglutida. Esta decisión no hace sino fortalecer la posición dominante de esta compañía en este mercado, aunque algunas nubes en el horizonte puedan hacer más imprevisible su futuro.
Termino aquí esta breve explicación sobre el caso de Rybelsus.
La llegada de la semaglutida oral supone un avance notable, pero debemos mantener una visión crítica sobre sus limitaciones y el contexto en el que se encuentra. La necesidad de dosis elevadas, las restricciones en la administración y el coste de producción plantean interrogantes sobre su viabilidad a largo plazo (por no hablar de la posible competencia). No obstante, Rybelsus es el claro ejemplo de que la ciencia aplicada puede encontrar soluciones ingeniosas a problemas complejos y sienta un gran precedente para la adopción de estos fármacos.
Nos vemos en el siguiente artículo.
Referencias
@BuckleyEtAl_2018_TranscellularStomachAbsorption @KimEtAl_2022_GastrointestinalPermeationEnhancers