Este es uno de esos errores de la ciencia que se descubren a posteriori y nos hacen darnos cuenta de lo ignorantes que somos y lo mucho que podemos estar equivocados.
Por suerte, este error no mató a nadie y se trata sólo de una graciosa coincidencia.
Esta es la historia de por qué se conoce a los glúcidos con el nombre de hidratos de carbono (y por qué esto es un error).
Los glúcidos
Los glúcidos son moléculas usadas como fuente de energía primaria por muchos seres vivos, incluidos los humanos, y comprenden sustancias como la glucosa, la fructosa, la sacarosa (el azúcar de las frutas o refinado) o la lactosa (el azúcar de la leche).
Estructura molecular de la glucosa.
Los motivos por los que estas moléculas son usadas como fuente de energía escapan a este texto, pero podríamos resumirlo en que los enlaces que conforman los glúcidos contienen mucha energía que puede ser aprovechada por nuestro cuerpo.
El caso es que, a mediados del siglo XIX, científicos como el químico Jean-Baptiste Dumas se encontraban estudiando la composición de distintas sustancias dulces. No conocíamos la estructura molecular de los glúcidos, pero estábamos haciendo avances.
Además de acuñar el término “glucosa”, que deriva del griego “glycos” (dulce, o vino dulce), Dumas descubrió que la composición de los glúcidos seguía la fórmula empírica:
Donde:
- es el número de átomos de Carbono de la molécula
- es el número de átomos de Oxígeno de la molécula
- es el número de átomos de Hidrógeno, que siempre era el doble que el de Carbono y Oxígeno
- es el número por el que se podían multiplicar estos átomos para conseguir glúcidos más sencillos o complejos.
Algunos glúcidos no siguen esta fórmula, pero ya sabemos que en ciencia nada es exacto y me estropearía la historia.
Así, por ejemplo, la fórmula de la glucosa sería:
Y la de la ribosa, otro glúcido que forma parte de nuestro ADN:
¿Cómo se obtuvo esta fórmula?
Empleando métodos químicos de la época, que consistían en:
- Quemar compuestos como la glucosa para determinar la proporción de carbono, hidrógeno y oxígeno que aparecía en sus productos de combustión, como el agua () y el dióxido de carbono ().
- Determinar el peso molecular aproximado de la molécula, lo que permitía, comparándolo con el peso de los átomos que la componían, hacer encaje de bolillos hasta que el peso de la molécula equivalía a la suma de los átomos que la componía.
Algunos ya os habréis dado cuenta de que la fórmula guarda una extraña relación.
Parecía que, por cada átomo de carbono , existía una molécula de agua . O dicho de otra forma, era como si los carbonos estuvieran hidratados por una molécula de agua en proporciones fijas: un carbono + una molécula de agua.
De esta mera casualidad de la relación estequiométrica surgió el nombre de Hidratos de Carbono (carbonos hidratados, o carbonos con agua) y fue introducido en nuestro vocabulario.
Por qué esto es un error.
Porque la fórmula empírica de una molécula, como la de la glucosa (), no nos dice nada sobre su estructura molecular y puede llevar a error. Por ejemplo, la fórmula empírica de la glucosa y la fructosa es la misma, pero su estructura es distinta.
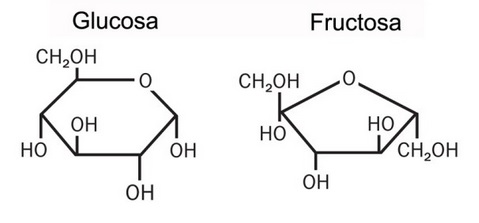
Pero no fue tras décadas después desde el descubrimiento de esta fórmula que se comenzaron a dilucidar las primeras estructuras moleculares de los azúcares, como la de la glucosa:
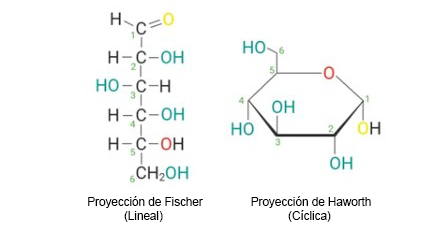
Y ahí fue cuando se empezaron a dar cuenta del error: Resultaba que los carbonos de los glúcidos no estaban hidratados. Si nos fijamos en el centro de la estructura de la izquierda con la proyección de Fischer, nos daremos cuenta de que los carbonos centrales no están unidos a una molécula de agua. De hecho, el propio Emil Fischer fue quien demostró que los glúcidos tenían estructuras complejas y no eran una simple combinación de carbono y agua.
No existía un átomo de carbono unido a una molécula de agua, sino que cada átomo de carbono se unía, por un lado, a un hidrógeno , y por otro, a un grupo hidroxilo .
La razón de que la fórmula estequiométrica funcionara se debía al mero azar, a la simple casualidad, y no guardaba relación con la estructura real de los glúcidos.
Sin embargo, para entonces el término ya se había popularizado y, a pesar del error, las contribuciones de Dumas a la química orgánica fueron revolucionarias y contribuyeron a comprender mucho sobre la composición de los azúcares.
De hecho, la RAE recoge el significado de azúcar de la siguiente manera:
Azúcar:
- Sustancia cristalina perteneciente al grupo químico de los hidratos de carbono, de sabor dulce y de color blanco en estado puro, soluble en el agua, que se obtiene de la caña dulce, de la remolacha y de otros vegetales.
- hidrato de carbono.
¿Y quién soy yo para contradecir a la RAE?