
Seguimos actualizando lo que sabemos sobre los anticuerpos en fase clínica de Abcellera.
Hoy le toca a ABCL575.
De acuerdo con los informes disponibles, este anticuerpo seguiría en fase 1 en la actualidad, con los resultados del estudio esperados para finales de 2026.
No es de extrañar que el ensayo esté siendo tan largo, ya que esperaban poder emplear una pauta de administración de una inyección cada 3-6 meses.
Indicación
ABCL575 está siendo desarrollado para tratar la dermatitis atópica (AD), una enfermedad autoinmune que se caracteriza por la inflamación y descamación de la piel a causa de una sobreactivación del sistema inmune.
Existen varios tratamientos aprobados que tratan de frenar la acción del sistema inmune, aunque todos entrañan riesgos debido a que la ventana terapéutica es muy pequeña: un exceso de inhibición del sistema inmunitario podría dejarte desprotegido frente a otras enfermedades potencialmente más peligrosas que la DA.
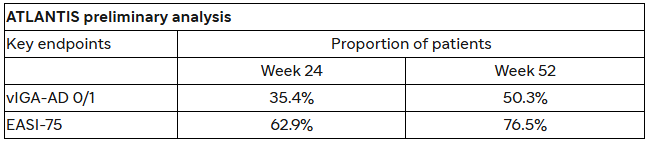
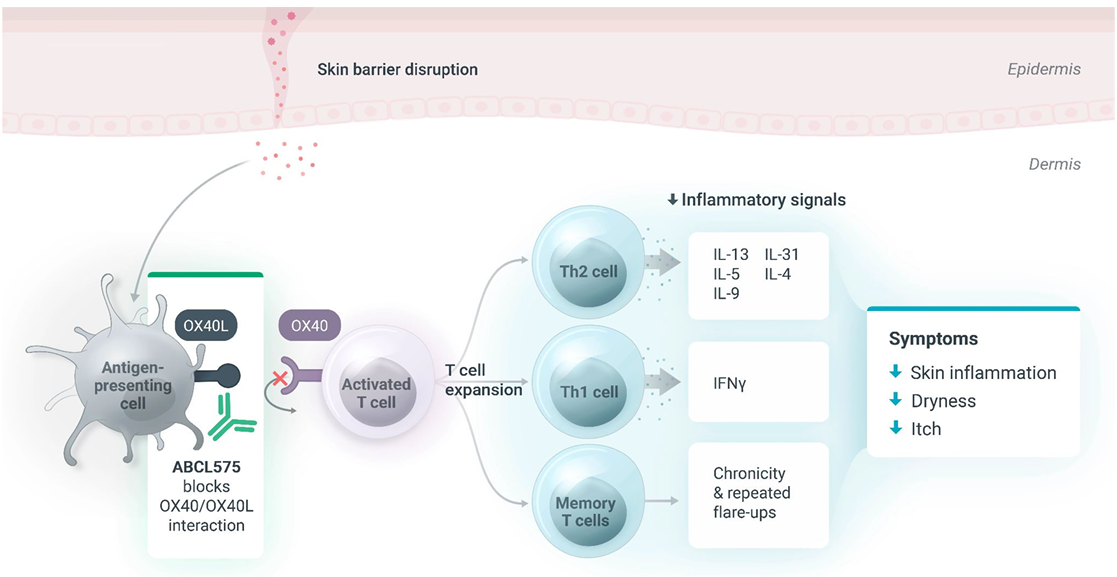 Fuente: Abcellera corporate presentation.
Fuente: Abcellera corporate presentation.
Los endpoints
Antes de empezar a comparar fármacos, tenemos que entender cómo se mide la eficacia de los mismos en DA.
Para evaluar terapias en DA se emplean dos criterios: vIGA-AD 0/1 y EASI-75.
No os asustéis con los nombres, que en realidad son sencillos de entender.
vIGA-AD 0/1
El validated Investigator Global Assessment for Atopic Dermatitis (vIGA-AD) es una escala estandarizada en la que el investigador puntúa la apariencia global de la piel del paciente en un momento dado. La escala puede ir desde 0 (normal) a 4 (grave).
En los ensayos de DA, se clasifica como “paciente o respondedor 0/1” a aquella persona que, tras finalizar el tratamiento, tiene una puntuación de 0 o 1 en sus lesiones. Las agencias regulatorias suelen exigir además una mejoría mínima de 2 puntos respecto a la situación basal, es decir, pasar de 3 a 1 o de 4 a 2, para considerar que la mejoría es relevante.
Esta medida es el criterio primario usado en muchos de estos ensayos porque es exigente y proporciona una medida global, sencilla y reproducible de la severidad de las lesiones.
EASI-75
El Eczema Area and Severity Index (EASI) es un criterio que cuantifica la gravedad y extensión de la DA dividiendo el cuerpo en 4 regiones (cabeza/cuello, tronco, extremidades superiores e inferiores). Cada región se puntúa por área afectada y severidad, con una puntuación que puede ir desde 0 a 72.
Se considera que un paciente es “respondedor EASI-75” cuando alcanza una reducción del 75% o más en la escala EASI tras haber finalizado el tratamiento.
El EASI-75 suele ser un endpoint coprimario frecuentemente solicitado por las agencias regulatorias en ensayos de DA junto con vIGA-AD 0/1.
En resumen, vIGA-AD evalúa de forma rápida y cualitativa la apariencia de la piel del paciente; EASI indica el tamaño y gravedad de las lesiones de manera cuantitativa. Ambas se usan de manera conjunta en ensayos clínicos.
Competidores
Antes de nada, tenemos que entender que las primeras terapias que se recomiendan para DA son los corticoesteroides tópicos o sistémicos —moléculas que reducen la respuesta inmune de manera generalizada.
Sin embargo, una cantidad considerable de pacientes encuentra que los corticoesteroides no son efectivos o no son la mejor opción a largo plazo.
En esa población donde los corticoesteroides no son una opción, tenemos varias alternativas como los inhibidores de las quinasas JAK, el metotrexato o la ciclosporina, pero cuyo uso está limitado a casos graves debido a sus efectos adversos.
Sin embargo, desde hace una década han aparecido tratamientos biológicos basados en anticuerpos, los cuales destacan por su alta especificidad y un buen perfil de seguridad y eficacia.
Dentro de los biológicos, tenemos un par de tratamientos aprobados:
- Dupilumab
- Tralokinumab
- Lebrikizumab
- Nemozilumab
Y otros tantos en desarrollo.
De los que están en desarrollo, nos centraremos en los que usan la misma diana farmacológica, el eje OX40-OX40L:
- Amlitelimab
- Rocatinlimab
- ABCL575
Por simplicidad, en este artículo compararemos Dupilumab —por ser el mejor de su clase y el tratamiento de primera opción— con los fármacos en desarrollo; incluido el de Abcellera.
La siguiente es su tabla comparativa:
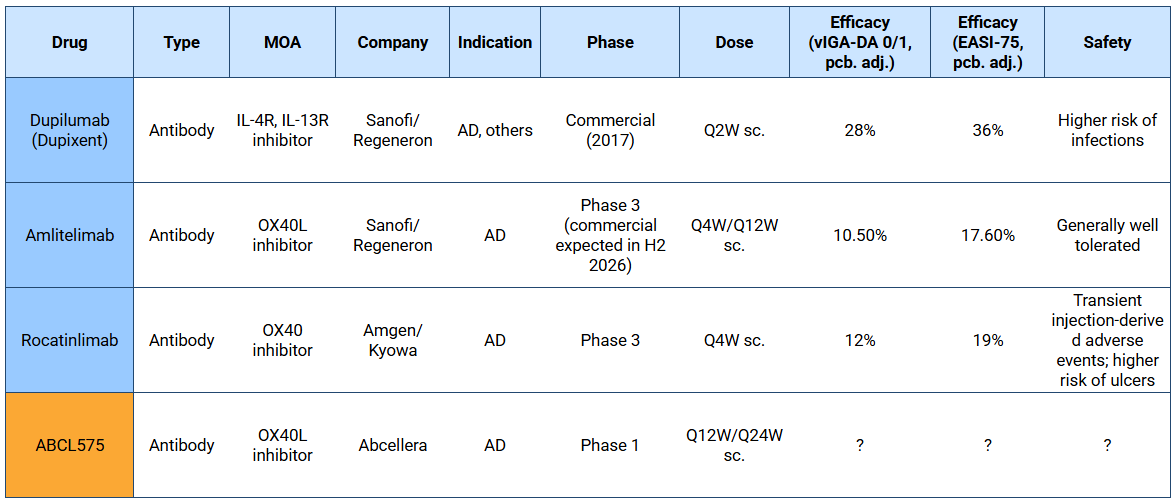
Todos los datos están ajustados al grupo placebo.
En estos ensayos se permite a los pacientes recibir “medicación de rescate” si sus síntomas de DA empeoran y el tratamiento no funciona. La medicación de rescate consiste en corticoides tópicos u orales para aliviar los síntomas. Eso sí, cuando un paciente recibe esta medicación es automáticamente catalogado como “no respondedor”, es decir, que se le cataloga como que no le ha funcionado el fármaco en investigación.
Dupilumab (Dupixent)
Dupilumab se trata de un anticuerpo que inhibe la subunidad alfa del receptor de IL-4 (IL-4Ra), con lo que impide la unión y señalización de IL-4 e IL-13. Estas interleuquinas son conocidas por sobreestimular al sistema inmune en DA, siendo la IL-13 especialmente relevante en la fisiopatología de la DA.
Desarrollado por Sanofi y Regeneron, Dupilumab es el líder absoluto del mercado. En 2024 este anticuerpo generó casi 15B $ en ventas globales considerando todas sus indicaciones aprobadas (DA, asma, CRSwNP, esofagitis eosinofílica, EPOC y prurigo nodularis). De estas, se estima que la DA representa aproximadamente la mitad de las ventas, lo que situaría a Dupilumab controlando en torno al 40% del mercado total de la DA y prácticamente la totalidad del segmento de los biológicos.
Los ensayos clínicos SOLO1 y SOLO2 muestran que Dupilumab es capaz de conseguir que un 28% de los pacientes alcancen el punto vIGA-AD 0/1 y un 36% el EASI-75 (respecto al placebo), lo que significa una mejoría significativa en la población con DA.
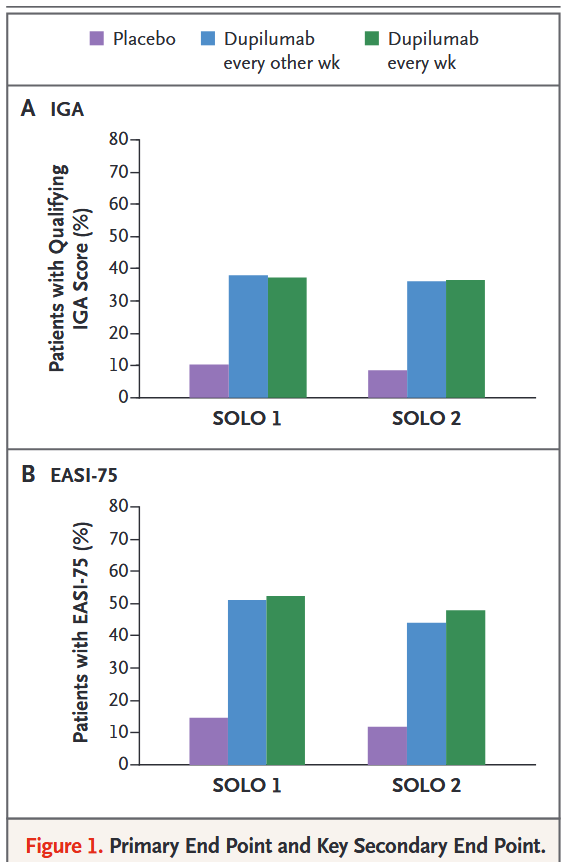
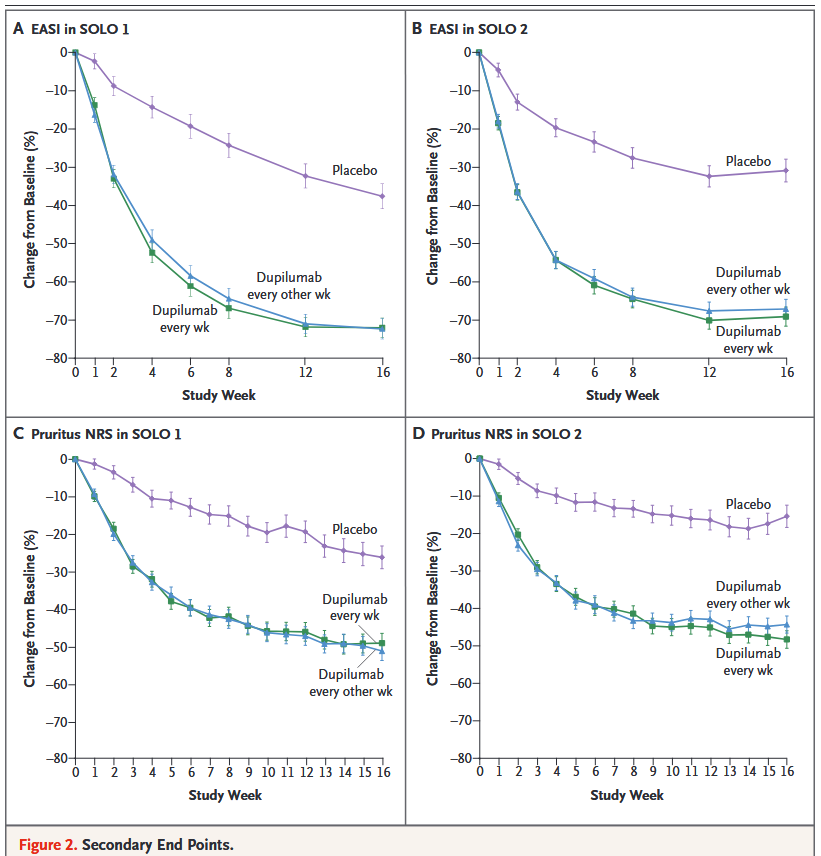
Nótese que en los ensayos se comparó una inyección subcutánea de Dupilumab cada semana vs. una cada dos semanas. Los resultados mostraron que no había diferencias entre ambas pautas, por lo que se comercializó la que se inyecta cada dos semanas.
El fármaco mostró un perfil de seguridad bastante bueno teniendo en cuenta que estamos inhibiendo al sistema inmune. Con solo un 2% de bajas en el ensayo, los mayores efectos adversos reportados fueron un mayor riesgo de infecciones, lo cual refleja el delicado equilibrio que existe al intentar modular el sistema inmune.
Siendo honestos, el éxito de Dupilumab pone el listón muy alto para el resto de terapias. La mayoría de pacientes continúan el tratamiento pasados varios años, síntoma de que el fármaco funciona y les permite llevar una vida mejor.
Pasamos ahora al nuevo eje OX40-OX40L (del que ya hablamos en el análisis de Abcellera Biologics).
Amlitelimab
Desarrollado también por Sanofi —en previsión de que las patentes de Dupilumab caducan en 2030—, Amlitelimab es una apuesta por combatir la DA a través de la inhibición de OX40L.
Los datos clínicos ya nos indican que su potencia es inferior a la de Dupilumab: los ensayos SHORE mostraron que Amlitelimab administrado cada 4 o 12 semanas podía conseguir que un 12-15% de los pacientes viera eliminada su dermatitis atópica en la semana 12 (según escala vIGA-AD 0/1 y ajustado al placebo).
Estos datos, de por sí inferiores a los de Dupilumab, ocultaban además que Amlitelimab se administraba de manera conjunta con corticoides tópicos, lo cual estaba disfrazando la eficacia real del tratamiento. En los ensayos COAST donde los pacientes sólo recibían Amlitelimab, los datos de eficacia a la semana 12 eran aún inferiores, y sólo un 10% de los pacientes lograban una remisión total de la DA.
Estos datos, que rozan la falta de mejoría significativa (y de hecho según criterios europeos no lo son), serían motivos suficientes para descartar el fármaco. No obstante, Sanofi espera su aprobación en Estados Unidos para la segunda mitad de 2026.
La explicación más probable es que, aun siendo una opción inferior a Dupilumab, es cierto que fue muy bien tolerado por los pacientes, y los ensayos a largo plazo (1 año vista) indican una mejoría sustancial de más pacientes. Sería una diana con buena eficacia, pero que tarda en hacer efecto:
Esto me lleva a pensar que con OX40L quizás estemos ante una situación calculada de riesgo-beneficio. Inhibir OX40L parece menos potente que inhibir las IL-4 e IL-13, pero quizás también deje menos expuesto tu sistema inmune para combatir infecciones. Dado que OX40L está implicado en las respuestas inmunes de largo plazo, inhibir esta proteína dejaría al resto del sistema funcionando y protegiendo frente a infecciones. Además, la dosificación cada 12 semanas implicaría que los pacientes sólo tendrían que recibir una inyección 4 veces al año.
Si el efecto a largo plazo de Amlitelimab aumenta y es persistente, y dado que la DA es una enfermedad crónica, es posible que Amlitelimab sea una opción viable para un porcentaje de la población.
Rocatinlimab
Rocatinlimab, desarrollado por Amgen y Kyowa, trata de atacar la otra parte de la vía OX40L-OX40. Este anticuerpo está diseñado para inhibir específicamente a OX40, el receptor de OX40L presente en los linfocitos T que se sobreactivan en DA.
Los resultados de los ensayos ROCKET de fase 3 resultan algo confusos por dos motivos:
- Se emplearon dos cohortes de pacientes: unos que ya habían probado anteriormente otros tratamientos fuertes para DA sin éxito y otros que no.
- Se reportan dos medidas de eficacia: la real y otra “maquillada” que es un cálculo de la potencia máxima que tendría este fármaco en una situación ideal.
Respecto a lo segundo, el cálculo es similar al Efficacy Estimand de los ensayos de obesidad. Como el resto de fármacos no lo reportan, usar esta medida para compararlos sería echarse trampas al solitario.
Los datos menos sesgados nos indican que la administración de Rocatinlimab cada 4 semanas conseguía que un 12% de los pacientes vieran una remisión de su DA a las 24 semanas. Esta cifra del 12% sigue quedando muy por debajo de Dupilumab y también de Amlitelimab, que alcanzaba esos números en la semana 12.
A esta aparente falta de diferenciación respecto a Amlitelimab se le suman los mayores efectos secundarios que provocó Rocatinlimab: hasta un 10% de los pacientes reportó fiebre, un 7% dolores de cabeza y un 4% la presencia de úlceras aftosas —lo que en términos coloquiales conocemos como aftas o llagas en la boca. La presencia de úlceras no se limitó a la boca, ya que un par de pacientes abandonaron el ensayo por úlceras ilíacas y gástricas.
*Aunque no sabemos por qué Rocatinlimab estaría provocando estas úlceras, una posible explicación es que el problema derive de la diana farmacológica.
Sin entrar en detalles porque ya vimos el mecanismo en el análisis de Abcellera, Amlitelimab inhibe OX40L y Rocatinlimab OX40, su receptor expresado en los linfocitos T.
Mientras que inhibir OX40L evita que los linfocitos T se activen, el bloqueo de OX40 podría estar induciendo una mayor depleción de linfocitos T activados. Si esta hipótesis fuera correcta, Rocatinlimab conseguiría una inmunosupresión más agresiva (al eliminar linfocitos T en lugar de simplemente evitar su activación), lo que podría explicar efectos adversos más pronunciados. Esta modulación más amplia del sistema inmune podría estar alterando poblaciones de linfocitos T más allá de los implicados en DA, derivando potencialmente en la aparición de úlceras. No obstante, esta explicación es especulativa y requeriría confirmación experimental.*
Algo que tampoco he comentado es el hecho de que se ha reportado un caso de sarcoma de Kaposi tanto con Amlitelimab como con Rocatinlimab. El problema parece estar producido por la inhibición del eje OX40L. Esto sería un efecto digno de un black box warning si se confirma que fue debido al tratamiento, lo cual es posible porque el sarcoma de Kaposi sólo es típico en personas inmunocomprometidas (era muy común en casos de SIDA). Un riesgo extra a la clase. Adam May lo explica aquí muy bien.
Poco después de la publicación de estos resultados Amgen anunció el fin de la colaboración con Kyowa para desarrollar Rocatinlimab y que el activo pasaría a ser propiedad exclusiva de Kyowa. Aunque Kyowa piensa seguir desarrollando Rocatinlimab, los datos que hemos visto y el hecho de que Amgen se haya desvinculado de este anticuerpo no me dan mucha confianza en que el fármaco vaya a llegar al mercado.
Frente a este panorama, surgen dudas respecto a ABCL575.
Los datos nos avisan de que inhibir OX40L no tiene la misma eficacia que inhibir las IL-4 e IL-13 como hace Dupilumab. Es cierto que ABCL575 podría ser más potente que Amlitelimab y sorprendernos en ese sentido, pero el hecho de que Rocatinlimab consiga una eficacia similar ya nos deja ver que quizás hay un máximo de eficacia terapéutica en la vía OX40L-OX40 que ya han alcanzado estos otros fármacos.
Por otro lado, ABCL575 podría ser una opción mejorada de Amlitelimab, que destaca por su seguridad y su eficacia a largo plazo. Si ABCL575 consigue una administración bianual como planean, podría convertirse en una opción cómoda y barata para el paciente. Sin embargo, tampoco representaría un gran cambio pasar de 4 a 2 inyecciones al año; la diferenciación debe ser mayor si aspiramos a que ABCL575 venda algo habiendo llegado 4-5 años más tarde al mercado.
Los comentarios de Carl Hansen respecto a ABCL575 irían por ese camino de conseguir el mismo efecto terapéutico reduciendo el número de inyecciones al año, lo que sería una diferenciación modesta:
“We view success in these trials as potential upside that support the proposition that OX40 ligand will emerge as a dominant class in treating autoimmune conditions. As compared to amlitelimab, the main differentiation thesis for ABCL575 is a combination of high potency and excellent biophysical properties, making it amenable to a high concentration formulation and an Fc that is engineered with a YTE mutation to provide extended half-life that supports less frequent dosing. We view this as a modest case for differentiation but one that could prove more or less important depending on what happens in ongoing trials with amlitelimab and the profile of other early stage OX40 ligand antagonists that are currently in late preclinical or early clinical development.”
Ahora bien, existe un factor adicional que podría jugar a favor de ABCL575: el precio. Dupilumab cuesta aproximadamente 37k $ al año, lo que limita su acceso en muchos sistemas sanitarios. Si ABCL575 logra demostrar eficacia comparable a Amlitelimab con una dosificación bianual, Abcellera podría posicionar el fármaco como una alternativa con mejor relación coste-eficacia. Una pauta de 2 inyecciones al año reduciría significativamente los costes de fabricación, distribución y administración comparado con las 26 inyecciones anuales de Dupilumab o las 4 de Amlitelimab. Además, llegar al mercado cuando las patentes de Dupilumab caduquen en 2030 podría permitir competir en precio contra biosimilares manteniendo diferenciación como producto innovador.
Como digo, todo esto son elucubraciones hasta que tengamos los primeros resultados de ABCL575 a finales de 2026, pero es bueno saber con qué cartas juegas.
Mercado
El mercado total de la DA alcanza los 17.6B . De estos, el segmento de los biológicos representa un 40% del mercado (casi totalmente controlado por Dupilumab).
Sin embargo, lo interesante de estas terapias es que su uso va más allá de la DA y se extiende a prácticamente cualquier indicación donde tengamos una sobreactivación del sistema inmune en la que esté implicado el eje OX40L-OX40 —que son muchas. Si sumamos el asma severo, la artritis reumatoide, el lupus eritematoso sistémico, la psoriasis, etc., podríamos fácilmente llegar a un mercado combinado potencial que supere los 50B $.
Si hacemos unos cálculos similares a los de ABCL635, podemos intentar estimar un pico de ventas para ABCL575.
El segmento de biológicos anti-OX40L podría capturar un 15-25% del mercado de biológicos en DA para 2032, lo que supondría unos 2.5-4.5B **, con un escenario base en torno a los 750M $.
Conclusiones
De los dos candidatos en clínica que tiene Abcellera, ABCL575 es el menos atractivo de los dos.
ABCL635 tiene una vía de diferenciación más clara y su mayor riesgo (eficacia y seguridad aparte) es el timing para llegar al mercado. ABCL575 compite contra anticuerpos prácticamente aprobados (Amlitelimab) y emplea la misma diana farmacológica y modo de acción, por lo que su única baza es justificar que su dosificación sea más dilatada en el tiempo —algo no demasiado alentador.
El valor de Abcellera no reside tanto en estos dos candidatos individuales sino en la plataforma de descubrimiento en sí misma, algo que sí validarán estos candidatos si demuestran ser opciones viables para sus indicaciones.
Un abrazo,
Gonzalo.